题目内容
小亮同学想通过实验探究某企业采用的氨碱法制的纯碱样品的成分及含量.
【提出问题】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,小亮做出如下假设:
(1)只含有Na2CO3;(2)含有Na2CO3和NaHCO3
【查阅资料】
(1)表中的现象Ⅰ为 ;
(2)现象Ⅱ对应的化学方程式为 .
【实验探究】为了确定纯碱样品的成分,小亮设计如下实验方案,请你一起完成下列实验报告.
【实验反思】实验步骤①中,氯化钙溶液过量的目的是 .
请你帮助小亮再设计一个实验方案来证明该样品中含有碳酸氢钠.
实验步骤
可能的现象 .
【提出问题】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,小亮做出如下假设:
(1)只含有Na2CO3;(2)含有Na2CO3和NaHCO3
【查阅资料】
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
(2)现象Ⅱ对应的化学方程式为
【实验探究】为了确定纯碱样品的成分,小亮设计如下实验方案,请你一起完成下列实验报告.
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量的CaCl2溶液. | 该反应的方程式: | |
| ②将上述反应后的混合液过滤,取滤液 | 有气泡产生 | 证明猜想②成立. |
请你帮助小亮再设计一个实验方案来证明该样品中含有碳酸氢钠.
实验步骤
可能的现象
考点:实验探究物质的组成成分以及含量,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:查阅资料:(1)稀盐酸可以和碳酸氢钠反应生成气体,可以据此解答该题;
(2)碳酸钠可以和氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,可以据此写出该反应的化学方程式;
实验探究:碳酸钠可以和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,可以据此写出该反应的化学方程式;碳酸氢钠和盐酸反应生成二氧化碳气体,可以据此完成实验现象;
实验反思:碳酸钠也可以和稀盐酸反应生成气体,为了防止碳酸钠干扰实验现象,所以应该加入过量的氯化钙将碳酸钠全部除去,可以据此解答该题;
根据碳酸氢钠溶液呈碱性,能使酚酞试液变红进行解答
(2)碳酸钠可以和氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,可以据此写出该反应的化学方程式;
实验探究:碳酸钠可以和氯化钙溶液反应生成碳酸钙沉淀和氯化钠,可以据此写出该反应的化学方程式;碳酸氢钠和盐酸反应生成二氧化碳气体,可以据此完成实验现象;
实验反思:碳酸钠也可以和稀盐酸反应生成气体,为了防止碳酸钠干扰实验现象,所以应该加入过量的氯化钙将碳酸钠全部除去,可以据此解答该题;
根据碳酸氢钠溶液呈碱性,能使酚酞试液变红进行解答
解答:解:查阅资料:(1)稀盐酸可以和碳酸氢钠反应生成气体,所以实验现象Ⅰ为产生了气泡;
(2)碳酸钠可以和氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,该反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
实验探究:碳酸钠可以和氯化钙溶液反应生成白色的碳酸钙沉淀和氯化钠,该反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl;碳酸氢钠和盐酸反应生成二氧化碳气体,所以加入稀盐酸后可以观察到有气泡冒出;
实验反思:碳酸钠也可以和稀盐酸反应生成气体,为了防止碳酸钠干扰实验现象,所以应该加入过量的氯化钙将碳酸钠全部除去;
碳酸氢钠溶液呈碱性,能使酚酞试液变红,所以实验方案是:实验步骤:取少量样品溶于水,加入过量的CaCl2溶液,将上述反应后的混合液过滤,取滤液滴加酚酞试液.
可能的现象:有白色沉淀产生;溶液变为红色.
故答案为:查阅资料:(1)产生气泡;
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
实验探究:
实验反思:将碳酸钠全部除去;
实验步骤:取少量样品溶于水,加入过量的CaCl2溶液,将上述反应后的混合液过滤,取滤液滴加酚酞试液.
可能的现象:有白色沉淀产生;溶液变为红色.
(2)碳酸钠可以和氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,该反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
实验探究:碳酸钠可以和氯化钙溶液反应生成白色的碳酸钙沉淀和氯化钠,该反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl;碳酸氢钠和盐酸反应生成二氧化碳气体,所以加入稀盐酸后可以观察到有气泡冒出;
实验反思:碳酸钠也可以和稀盐酸反应生成气体,为了防止碳酸钠干扰实验现象,所以应该加入过量的氯化钙将碳酸钠全部除去;
碳酸氢钠溶液呈碱性,能使酚酞试液变红,所以实验方案是:实验步骤:取少量样品溶于水,加入过量的CaCl2溶液,将上述反应后的混合液过滤,取滤液滴加酚酞试液.
可能的现象:有白色沉淀产生;溶液变为红色.
故答案为:查阅资料:(1)产生气泡;
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
实验探究:
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量的CaCl2溶液. | 有白色沉淀产生; | 该反应的方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| ②将上述反应后的混合液过滤,取滤液 滴加稀盐酸. | 有气泡冒出; | 证明猜想②成立. |
实验步骤:取少量样品溶于水,加入过量的CaCl2溶液,将上述反应后的混合液过滤,取滤液滴加酚酞试液.
可能的现象:有白色沉淀产生;溶液变为红色.
点评:解答这类题目时,首先,赏析问题情景,找到实验探究的反应原理;再根据实验的反应原理,分析推断出该物质的组成成分,然后得出所要探究的物质中该成分的组成.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目

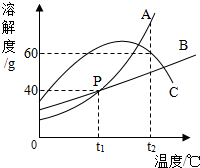 如图所示为A、B、C三种可溶物的溶解度曲线.结合图示回答以下问题.
如图所示为A、B、C三种可溶物的溶解度曲线.结合图示回答以下问题.