题目内容
【题目】如图为六种粒子的结构示意图。请回答下列问题:
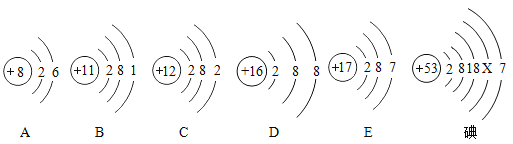
(1)图中不同种元素之间的本质区别是__________;
(2)A元素在与其他元素形成化合物时的化合价通常是___________(填化学用语);C元素的原子形成的离子是_______________(填离子符号);
(3)从原子结构上分析,图中_________(填元素符号)两种元素具有相似的化学性质;
(4)在上述碘的原子结构示意图中,x=__________;
(5)由B、D两种元素组成的化合物的化学式是_______________。
【答案】质子数不同(或核电荷数不同) ![]() Mg2+ Cl和I 18 Na2S
Mg2+ Cl和I 18 Na2S
【解析】
(1)元素是具有相同质子数的同类原子总称,所以不同种元素之间的本质区别是质子数不同或核电荷数不同;
(2)A元素(8号元素是氧元素)的原子最外层有6个电子,在化学反应中易得到2个电子而显-2价,化合价表示为在元素符号的正上方标注化合价的正负与数值,符号表示为:![]() ;C元素的原子最外层有2个电子,在化学反应中易失去2个电子形成带有2个单位正电荷的镁离子--Mg2+;
;C元素的原子最外层有2个电子,在化学反应中易失去2个电子形成带有2个单位正电荷的镁离子--Mg2+;
(3)从原子结构上分析,氯与碘原子的最外层的电子数相同,元素具有相似的化学性质,元素符号分别为:Cl和I;
(4)在原子中,质子数=核外电子数,所以53=2+8+18+X+7,X=18;
(5)B是11号元素--钠元素,在化合物中显+1价,D是16号元素--硫元素,在化合物中显-2价,所以二者组成的化合物的化学式为Na2S。

 阅读快车系列答案
阅读快车系列答案【题目】化学就在我们身边,它能改善我们的生活。根据所学知识回答:
(1)某矿泉水的主要矿物质成分及含量如下表:
成分 | Ca | K | Zn | F |
含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
这里Ca、K、Zn、F是指__________(填“单质、元素、分子或原子”)。
(2)我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有__________功能;
(3)超市里的一些食品采用真空包装,其原理是除去食品袋里的空气,使微生物因缺少______而受到抑制,达到防腐的目的;
(4)公共场所常用“84消毒液”(NaClO溶液)进行环境杀菌。NaClO中Cl元素的化合价是_________;
(5)茶杯内的纱网,可将茶叶与茶水分离,便于饮用,该设计利用的是化学实验操作中的________法;
(6)冬日里,我们可以利用木炭燃烧放出的热量,进行取暖。请写出木炭在空气中充分燃烧的化学方程式: _____________;
(7)喝酒不开车,开车不喝酒”,让司机向酒精检测仪吹气,通过显示的颜色变化,交警可快速测出司机是否酒后驾车.其反应原理为:2CrO3(红色)+3C2H5OH+3H2SO4===Cr2(SO4)3(绿色)+3CH3CHO+6X,该反应中X的化学式为_______(填选项字母)。
A:H2CO3 B:H2O C:CO D:SO