题目内容
下图为某化工企业生产流程示意图: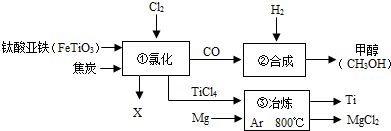
下列说法正确的是
| A.钛酸亚铁(FeTiO3)中钛元素为+3价 |
| B.①中反应方程式为:2FeTiO3+6C+7Cl2一定条件2X+2TiCl4+6CO,则X为FeCl3 |
| C.②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2 |
| D.③中氩气(Ar)作保护气,反应类型为复分解反应 |
B
解析试题分析:A.设FeTiO3中Ti的化合价是x.FeTiO3中Fe的化合价是+2价,O的化合价是-2价,利用化合物中各元素的化合价的代数和为零的原则可得(+2)+x+(-2)×3=0,解得x="+4" 所以钛酸亚铁(FeTiO3)中钛元素的化合价是+4价,故说法错误;B.根据质量守恒定律,在反应前后各元素原子的个数不变.从2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO看钛原子、氧原子、碳原子反应前后除物质x外个数已经相等,故x中无钛原子、氧原子、碳原子;反应前铁原子为2个,反应后只有x有,所以2x中有2个,从而x中有1个;反应前氯原子有14个,反应后x除外有8个,所以2x中有6个,因此x中有3个,因此x的化学式是FeCl3,故说法正确;C. 根据从化学方程式CO+2H2═CH3OH,结合化学方程式的意义可知一氧化碳和氢气的质量比是:28:4=7:1,故说法错误;D.由图示可知,TiCl4与Mg反应的反应物是TiCl4与Mg,生成物是Ti和MgCl2,该反应符合“单+化→单+化”的特点,为置换反应,故说法错误.
考点:物质的相互转化和制备;元素化合价的计算;基本反应类型;质量守恒定律及其应用

铬(Cr)是一种重要的金属材料,它具有良好的金属光泽和抗腐蚀性,常用来镀在其他金属的表面上,铜、铬、锰、镍组成合金可以制成各种性能的不锈钢。某校化学研究小组对Cr(铬)、Al、Cu的金属的活动性顺序进行探究,过程如下:
(1)[作出假设]对三种金属的活动性顺序提出三种可能的假设是:
①Cr>Al>Cu②Al>Cr>Cu③Cr>Cu>Al
[设计实验]同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象,记录以下:
| 金属 | Cr | Al | Cu |
| 与盐酸反应现 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无气泡产生,金属无变化 |
[控制实验条件]三种金属加入盐酸前都先用纱布将其表面擦光亮,其目的是 。
A.除去氧化膜,利于直接反应
B.使表面光亮,易观察现象
C.使金属温度相同,易反应
[得出结论]原假设中正确的是 (选填假设中①、②,③)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式 。
[结论应用]根据探究结果,请你预测铬与硫酸铜溶液 (填“能”或“不能”)反应,理由是 。
早在春秋战国时期,我国就开始生产和使用铁器。
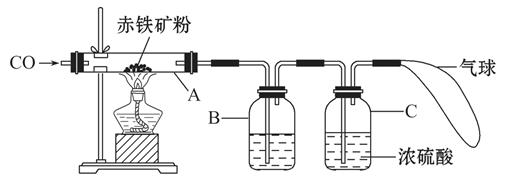
(1)写出用CO和赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式 ,盛水的铁锅与水面接触的一圈最易生锈,钢铁生锈的条件是 ,利用新技术能将不锈钢加工成柔软的金属丝,这是利用了不锈钢的 (填字母)。
| A.耐腐蚀性 | B.延展性 | C.导热性 | D.导电性 |
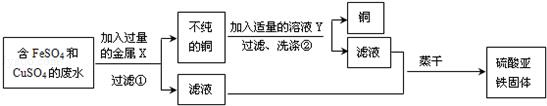
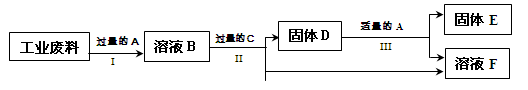
金属X是 ,写出上述实验方案中有关反应的化学方程式
① ;② 。
(12分)碱式碳酸盐广泛应用于工农业生产。
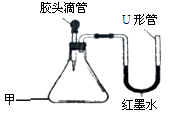
(1)某碱式碳酸盐样品M(OH)2·MCO3,为确定金属M的相对原子质量,某研究小组设计如下实验装置及步骤(不考虑植物油中溶解CO2产生的影响)。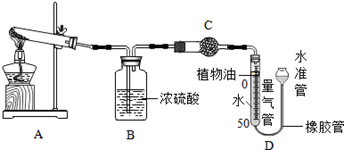
①连接装置并 ;②准确称量样品的质量;③装药品,调节量气装置两边液面相平,读数;④加热至样品质量不再减少;⑤冷却到室温;⑥调节量气装置两边液面相平,读数、列式计算。
Ⅰ.请将上述实验步骤补充完整;
Ⅱ.装置B的作用是 ,少量植物油的作用是 ,C中的试剂是 (填字母序号);
a.碱石灰 b.浓硫酸 c.硫酸铜
Ⅲ.步骤⑥中调节液面相平的操作是将水准管 (填“缓慢上移”或“缓慢下移”)。
Ⅳ.若其他操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是 (填字母序号);
a.反应前量气管水面在0刻度处,反应后仰视读数
b.样品未分解完全即停止实验
c.量气管中未加植物油
(2)实际生产中的碱式碳酸铜可表示为Cu(OH)2·mCuCO3,某研究小组仍使用上述装置测定m的值,测得3组数据如下表所示。取3组数据的值得到CO2的体积为 mL,又知常温常压下CO2的密度为1.964 g/L,据此计算m的值。(写出计算m的过程,最后结果保留小数点后两位) 。
| 组别 | 样品质量 | CO2体积 |
| 第1组 | 0.21 g | 22.39 mL |
| 第2组 | 0.21 g | 22.41 mL |
| 第3组 | 0.21 g | 22.40 mL |