题目内容
【题目】某校学习小组进行含氟牙膏是否能有效预防龋齿的实验探究。
信息:①蛋壳主要成分是CaCO3,其他成分对实验影响忽略不计。
②鸡蛋壳与牙齿和含氟牙膏反应的化学原理相似。
(实验一)(1)将新鲜的鸡蛋放在盛有足量稀盐酸的烧杯中,可观察到鸡蛋表面产生气泡,检验产生气泡成分的方法是_____(用化学方程式表示)。
(实验二)鸡蛋壳代替牙齿探究含氟牙膏能否预防龋齿。
查资料知,含氟牙膏(含氟成分为NaF)可与蛋壳反应,在表面生成氟化钙保护层。反应的化学方程式为:CaCO3+2NaF==CaF2+Na2CO3
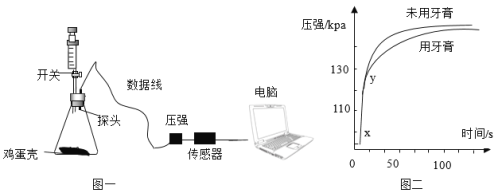
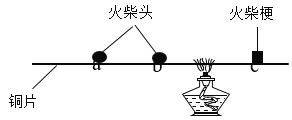
(2)按图一连接好装置,先检查装置气密性,方法是_____,再称取0.50g“牙膏处理过的蛋壳(用牙膏液浸泡、洗涤、晾干)”于锥形瓶中,用注射器抽取20mL稀盐酸(模拟形成龋齿的酸境),连接好装置,打开开关,将盐酸快速压入锥形瓶,关闭开关,测得压强随时间的变化如图二所示。用“未用牙膏处理的蛋壳”重复上述实验。(注:不考虑加入液体造成的压强差)
(3)图二中x-y段压强增大的主要原因_____。用“未用牙膏处理的蛋壳”重复上述实验的作用是_____。
(4)根据实验二的数据分析,含氟牙膏_____(填“能”或“不能”)预防龋齿,理由_____。
【答案】Ca(OH)2+CO2=CaCO3↓+H2O 打开开关,拉动(或推动)注射器活塞,松开后,活塞回到原位,说明气密性良好 碳酸盐同盐酸反应产生了二氧化碳气体,使瓶内压强增大 对比 能 相同条件下,使用含氟牙膏处理后的鸡蛋壳,反应产生的气体更少,压强更小,消耗的鸡蛋壳更少
【解析】
(1)鸡蛋壳中含有碳酸钙,将新鲜的鸡蛋放在盛有足量稀盐酸的烧杯中,发生化学反应生成二氧化碳,检验二氧化碳用澄清石灰水,检验二氧化碳的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(2)检查该装置气密性的方法是:打开开关,拉动(或推动)注射器活塞,松开后,活塞回到原位,说明气密性良好。
(3)密闭容器内气体增多,压强变大。图二中x-y段压强增大的主要原因是碳酸盐同盐酸反应产生了二氧化碳气体,使瓶内压强增大。用“未用牙膏处理的蛋壳”重复上述实验的作用是对比,以探究含氟牙膏能否预防龋齿。
(4)根据实验二的数据分析,含氟牙膏能预防龋齿,理由是相同条件下,使用含氟牙膏处理后的鸡蛋壳,反应产生的气体更少,压强更小,消耗的鸡蛋壳更少。

 阅读快车系列答案
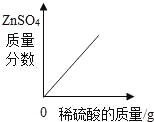
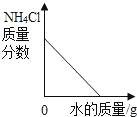
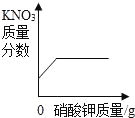
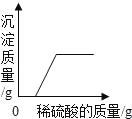
阅读快车系列答案【题目】下列图象与所述实验相符的是( )
A | B | C | D |
向一定量锌粒中加入过量稀硫酸 | 向一定量氯化铵饱和溶液中不断加入水 | t℃时,向一定量不饱和的硝酸钾溶液中不断加入硝酸钾晶体 | 向一定量氢氧化钠和氢氧化钡的混合溶液中加入稀硫酸 |
|
|
|
|
A. AB. BC. CD. D