题目内容
【题目】硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂。以下是由废铜料(含铁)生产硫酸铜晶体的流程。
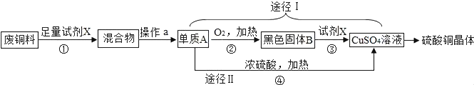
(1)B的化学式为_____,操作a的名称是_____。玻璃棒的作用_____
(2)②的反应基本类型为_____;反应①的化学方程式为_____;
(3)若试剂X为稀硫酸,写出反应③的化学方程式_____;
(4)已知:Cu+2H2SO4 (浓)![]() CuSO4+SO2↑+2H2O.环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生有害气体和_____。
CuSO4+SO2↑+2H2O.环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生有害气体和_____。
【答案】CuO 过滤 引流 化合反应 Fe+H2SO4═FeSO4+H2↑ CuO+H2SO4=CuSO4+H2O 硫酸的利用率高
【解析】
(1)黑色固体为金属铜在加热条件下与氧气化合产生的氧化铜;操作a为过滤操作,把不与稀硫酸反应的金属铜与硫酸亚铁溶液分离开来;其中玻璃棒的作用是引流;
(2)反应②,加热条件下金属铜与氧气化合生成氧化铜,是化合反应;反应①则是铁与硫酸铜反应生成硫酸亚铁和铜;化学方程式为: Fe+H2SO4═FeSO4+H2↑;
(3)反应③为黑色氧化铜与稀硫酸反应生成硫酸铜和水;化学方程式为:CuO+H2SO4=CuSO4+H2O;
(4)途径II产生的二氧化硫既会污染环境,又使硫酸不能全部转化为产品硫酸铜而形成浪费。

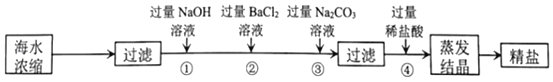
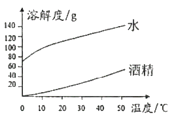
【题目】NaOH、Na2CO3分别在水、酒精中的溶解度如下表所示,结合图表数据下列说法正确的是
| NaOH | Na2CO3 | ||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |
A. 图表示Na2CO3在水、酒精中的溶解度曲线
B. 将CO2通入所得NaOH的酒精溶液中,无明显现象
C. 40℃时,将50gNaOH投入到100g酒精中,形成饱和溶液
D. 20℃升到40℃时,NaOH在水中的溶解度变化大于Na2CO3在水中的溶解度变化
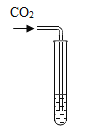
【题目】化学实验活动课上,同学们利用了如图所示实验探究氢氧化钙的性质。
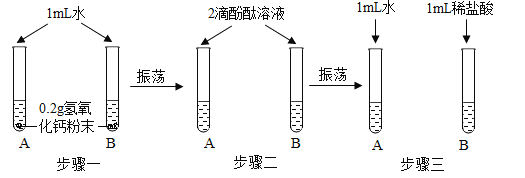
(1)上述三个步骤的A试管中固体始终无明显减少,那么能说明A试管的水中溶有氢氧化钙的现象是__________。
(2)步骤三试管B中溶液变无色,发生反应的化学方程式_______________。
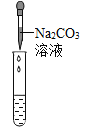
小明的实验:小明直接把稀盐酸滴入盛有氢氧化钙溶液的试管中,始终没有看到明显变化。
(提出问题)小明实验后试管中溶质的成分是什么?
(查阅资料)CaCl2溶液显中性。
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想I:只有CaCl2猜想Ⅱ有________
猜想Ⅲ:有CaCl2和Ca(OH)2
猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是_____________
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊试液 | 通入CO2 | 滴加Na2CO3 |
实验操作 |
|
|
|
实验现象 | _________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(评价反思)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_____________。