题目内容
同学们从山上采集到一种石灰石,他们取80g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得完全反应后剩余固体的质量为58g.求:该石灰石样品中CaCO3的质量分数,写出计算过程.
分析:煅烧石灰石时碳酸钙分解放出二氧化碳而使反应后固体质量减小,直到碳酸钙完全分解,剩余固体质量不再改变;利用质量守恒定律,由反应前后固体质量差计算出反应放出二氧化碳的质量,然后由反应的化学方程式,利用放出二氧化碳的质量求得石灰石样品中所含碳酸钙的质量,从而计算出样品中碳酸钙的质量分数.
解答:解:(1)由题中数据根据质量守恒定律可知生成二氧化碳的质量=80g-58g=22g;
设80g石灰石中含CaCO3的质量为x
CaCO3
CaO+CO2↑
100 44
x 22g
=
解得:x=50g
石灰石样品中CaCO3的质量分数为:
×100%=62.5%
答:该石灰石中CaCO3的质量分数为62.5%.
设80g石灰石中含CaCO3的质量为x
CaCO3
| ||
100 44
x 22g
| 100 |
| x |
| 44 |
| 22g |
解得:x=50g
石灰石样品中CaCO3的质量分数为:
| 50g |
| 80g |
答:该石灰石中CaCO3的质量分数为62.5%.
点评:本题难度不是很大,主要考查了根据化学方程式进行相关的计算,从而培养学生的分析能力和计算能力.

练习册系列答案
相关题目
同学们从山上采集到一种石灰石,他们取80 g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如表:
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为 g.
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
(3)请在如图所示的坐标图中,画出煅烧时生成气体的质量(m)随时间(t)变化的曲线.
| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |

(1)当石灰石完全反应后,生成CO2的质量为
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
(3)请在如图所示的坐标图中,画出煅烧时生成气体的质量(m)随时间(t)变化的曲线.
同学们从山上采集到一种石灰石,他们取80克该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为 g.
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
(1)当石灰石完全反应后,生成CO2的质量为
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
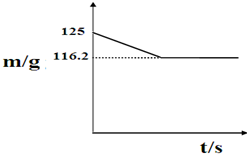 兴趣小组的同学们从山上采集到一种石灰石(主要成分为碳酸钙),他们将25克该样品放入盛有100g稀盐酸的烧杯中,恰好完全反应(杂质不与稀盐酸反应,也不溶于水),测得反应后烧杯中剩余物质的质量(m)与反应时间(t)的关系如图:
兴趣小组的同学们从山上采集到一种石灰石(主要成分为碳酸钙),他们将25克该样品放入盛有100g稀盐酸的烧杯中,恰好完全反应(杂质不与稀盐酸反应,也不溶于水),测得反应后烧杯中剩余物质的质量(m)与反应时间(t)的关系如图: