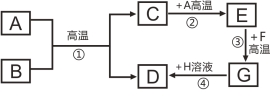
题目内容
【题目】某同学利用以下药品:长、宽和厚度均相同的锌片、铁片与铜片、稀硫酸、硫酸亚铁溶液、硫酸铜溶液、硫酸锌溶液、锌粉,验证锌、铁、铜的金属活动性顺序.
(1)实验前,用砂纸打磨金属片的目的是 ;
(2)根据实验目的,该同学设计了实验I、Ⅱ两种合弹的方案,如图l所示:
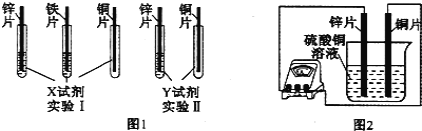
若X、Y是两种不同的试剂,则X、Y中溶质的化学式依次为 、 ;
(3)该同学将硫酸亚铁溶液和硫酸铜溶液混合在一起,溶液呈现青色.
A.向混合液中加入过量锌粉,搅拌,溶液颜色的变化应为:青色变浅至 色,最终变为无色;
B.向混合注中插人锌片,待其浸没部分表面完全变色后,溶液仍为青色,取下锌片表面附着的粉末,经检验其组成为铁和铜.粉末中存在铁的原因:
①反应生成了铁,写出该反应的化学方程式: ;
② ;
(4)如图2所示,该同学用导线将锌片和铜片连接起来,接入电流表,然后把它们一起插入硫酸铜溶液中,该实验的现象为:①电流表 ;②铜片表面 .
【答案】(1)除去金属表面的氧化膜 ;
(2)H2SO4 、 FeSO4 ;
(3)A.浅绿色 ;B.①Zn+FeSO4=ZnSO4+Fe ;
②铜和锌构成原电池,电子转移过程中亚铁离子得到电子变成铁单质 ;
(4)①指针发生偏转 ;②变粗
【解析】
试题分析:(1)金属在空气中其表面能生成一层氧化膜,氧化膜会阻止金属与药品的接触,所以要先除去氧化膜;
(2)实验1:给定三种金属,因此可以和酸混合:将三种金属分别于稀硫酸混合后,铜与稀硫酸不反应,锌、铁均能与稀硫酸反应产生气体,且锌的反应比铁剧烈,可以得出锌>铁>铜;
实验2,给定两种金属,可以和中间金属的盐溶液混合,由于锌能与硫酸亚铁反应,说明锌在铁的前面,铜不与硫酸亚铁反应,说明铁在铜的前面.所以可以选用的另外一种药品是硫酸亚铁溶液;
(3)A、硫酸亚铁溶液是浅绿色,硫酸铜溶液是蓝色,离子溶液混合后呈现青色,加入过量锌粉后,先和硫酸铜发生置换反应,青色变浅;硫酸铜完全反应后,溶液变为浅绿色;接着锌再和硫酸亚铁发生置换反应,变成硫酸锌,溶液呈现无色;
B、混合盐溶液中插入锌片,铁单质可能有离子来源:当溶液中铜离子的浓度很稀时,锌与硫酸亚铁直接发生置换反应,反应的方程式为:Zn+FeSO4=ZnSO4+Fe;也可能是铜和锌构成原电池,电子从锌片转移到铜片上时,溶液中的铜离子、亚铁离子得到电子变成铜单质和铁单质;
(4)原电池中锌比铜活泼,所以锌失去电子,电子从锌片流向铜片,而电流从铜片流向锌片,所以电流表指针发生偏转;铜离子在铜片上得到电子,生成红色的铜单质,故锌片变薄,铜片表面变粗.

【题目】某化学课堂上同学们正在进行酸、碱、盐知识的探究,以下是教学片断,请你参与其中并认真填写空格.
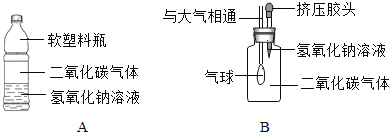
【学生实验】将二氧化碳分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.
【学生板演】澄清石灰水变浑浊的原理 (用化学方程式表示)
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想①:两者发生了化学反应;猜想②:两者没有发生化学反应
【实验探究】
(1)小华设计了如图所示的A、B两个实验.
实验现象:A中软塑料瓶変瘪,B中
(2)小红认为小华的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低.小明同学却对此提出质疑,他认为小华的实验不严谨,其理由是 ,要得到科学严谨的结论,仍利用该装置,补做的对比实验是 .
(3)小宁设计的是通过检验生成物来验证猜想,请帮她填写实验报告.
实验步骤 | 实验现象 | 实验结论 |
向B实验后的溶液中加入 | 验证了二氧化碳和氢氧化钠溶液反应 |
【实验结论】二氧化碳和氢氧化钠溶液发生了反应.
【反思拓展】通过此探究实验,我们发现,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是 ; .