题目内容
钢铁的锈蚀主要是铁与空气中的 、 等物质发生化学反应的结果,铁绣的主要成分是 (写化学式).金属属于 (填“再生”或“不可再生”)资源,废旧金属属于 (填“可回收”或“不可回收”)垃圾,解决金属腐蚀以及有效利用废旧金属的问题,既可以节约资源,又能实现节能减排.请说出一种防止铁制品锈蚀的具体方法 .
考点:金属锈蚀的条件及其防护,铁锈的主要成分,金属的回收利用及其重要性
专题:金属与金属材料
分析:根据铁锈蚀的条件、铁锈的主要成分及金属资源回收利用及防止锈蚀的等知识分析回答.
解答:解:钢铁的锈蚀主要是铁与空气中的氧气、水等物质发生化学反应的结果,钢铁锈蚀后生成铁锈(主要成分是氧化铁).金属属于可再生资源,废旧金属属于可回收垃圾,防止铁制品锈蚀的方法有在铁制品表面刷保护漆,防止铁制品受潮等;
故答为:氧气;水;Fe2O3;再生;可回收;在铁制品表面刷保护漆.
故答为:氧气;水;Fe2O3;再生;可回收;在铁制品表面刷保护漆.
点评:本题重在重在考查身边化学,更加贴近生活和生产,可以使学生感受到“生活处处有化学”.这也是中考的题型之一.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
又到了炎炎夏日,专家提醒:在夏天勿将打火机、空气清新剂等易燃物品留在车内,防止温度过高使它们成为汽车自燃的元凶.打火机的主要燃料是丁烷(C4H10).下列说法不正确的是 ( )
| A、拿走车内的打火机、空气清新剂、抽纸等物品,目的是通过去除可燃物防止燃烧发生 |
| B、从结构上看:一个丁烷分子由4个碳原子、5个氢分子构成 |
| C、汽车发生自燃时,某些车主冒然打开车门或引擎盖,燃烧更加剧烈,是因为提供了更多的氧气 |
| D、某些车辆自燃时甚至引起爆炸,是因为可燃物在有限的空间剧烈燃烧导致的 |
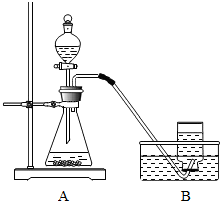 某同学用双氧水和二氧化锰来做制取氧气的实验.请回答下列问题.
某同学用双氧水和二氧化锰来做制取氧气的实验.请回答下列问题.
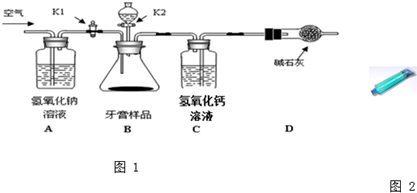 牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分如图2.
牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分如图2.