题目内容
【题目】用如图所示的三组实验来探究二氧化碳的性质:
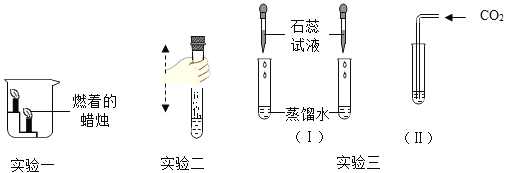
①在实验一中,将一瓶二氧化碳沿烧杯内壁慢慢倒入小烧杯中,可以观察到的现象是_____,由此可以得出二氧化碳的性质是______。
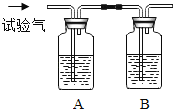
②实验二中,向集满CO2的试管内倒入约占试管容积三分之一的澄清石灰水,旋紧胶塞,持续振荡一定时间,试管中发生反应的化学方程式是______,充分振荡后,试管内压强_____试管外大气压强(填“>”或“=”或“<”)。
③实验三中加入石蕊试液的目的是____,然后向其中一支试管中通入二氧化碳,溶液变____色,反应的化学方程式为______;本实验中用两只试管的目的是_____。
【答案】下层的蜡烛先熄灭,上层的蜡烛后熄灭 密度比空气大,不可燃也不支持燃烧 CO2+Ca(OH)2=CaCO3↓+H2O < 检验CO2是否与水发生化学反应 红 CO2+H2O═H2CO3 对照
【解析】
在实验一中,将一瓶二氧化碳沿烧杯内壁慢慢倒入小烧杯中,可以观察到的现象是:下层的蜡烛先熄灭,上层的蜡烛后熄灭,由此可以得出二氧化碳的性质有:密度比空气大,不可燃也不支持燃烧;
②实验二中,向集满CO2的试管内倒入约占试管容积三分之一的澄清石灰水,旋紧胶塞,持续振荡一定时间,会看到澄清石灰水变浑浊,原因是二氧化碳与石灰水发生反应生成了碳酸钙沉淀,其化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;反应后由于密闭容器内的二氧化碳被消耗,所以容器内气压减小,
③实验三中,先分别向两支盛有蒸馏水的试管中滴加几滴紫色石蕊试液,然后向其中一支试管中通入二氧化碳,会发现实验(Ⅱ)中溶液变红色,原因是二氧化碳溶于水生成了碳酸,碳酸能使紫色石蕊试液变红,其反应的化学方程式为 CO2+H2O═H2CO3。
故答案为:①下层的蜡烛先熄灭,上层的蜡烛后熄灭;密度比空气大,不可燃也不支持燃烧;②CO2+Ca(OH)2=CaCO3↓+H2O;<;③检验二氧化碳是否与水发生化学反应;红; CO2+H2O═H2CO3;对照。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案