��Ŀ����
����Ŀ��С��ͬѧ��ʵ��̽������þ��ͭ���ֽ����Ļ��˳��ʱ�����йط�Ӧ��¼���£�
Fe+2HCl=FeCl2+H2�� Mg+2HCl=MgCl2+H2�� Fe+CuSO4= FeSO4+Cu Cu+2HCl![]() ����Ӧ
����Ӧ
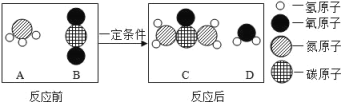
��1����������Ӧ�У��ɻ�õ���Ϣ�У�����������____________��
��2��ͨ���۲�ʵ��������˵��þ�������õ�������____________���������һ��ʵ�飨�û�ѧ����ʽ��___________��Ҳ��˵��þ�������á�
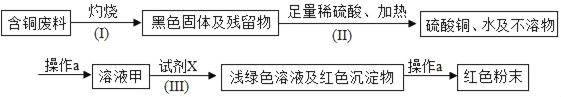
��3���ý����˳����������е�һЩ�����磺_____________
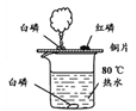
��4��ʹ���������������彡������Ҫԭ����______________
��5�����Ǵ���ʹ�õ��ǺϽ�������Ϊ�Ͻ���и����������ܣ���ֱȴ�����Ӳ��_____
���𰸡����Ľ�����ǿ��ͭ��þ�Ľ�����ǿ��ͭ�����Ľ�����ǿ��ͭ�ȣ� þ�����ᷴӦ���ʿ죬��Ӧ���ң�Ѹ�ٲ����������� FeCl2+Mg=MgCl2+Fe �������⣬ͭ�������� ������ʳ���к���������Ҫ����Ԫ�� ��
��������
��1����Fe+2HCl�TFeCl2+H2����֪�����Ļ����Դ����⣬��Fe+CuSO4�TFeSO4+Cu��֪�����Ļ����Դ���ͭ�ȣ�
��2������þ�����ᷴӦ�����ʱ����죬˵����þ�������á�ͨ��þ��������������Ӧ��Ҳ˵����þ�������ã���Ӧ�ķ���ʽ�ǣ�FeCl2+Mg=MgCl2+Fe��
��3��������Һ����Ҫ�ɷ�Ϊ����ͭ����������Ͱװ����Ϊ�����û���ͭ����ʴ��Ͱ����ʹ������ҺʧЧ�����������⣬ͭ�������⣻
��4��ʹ���������������彡������Ҫԭ����������ʳ���к���������Ҫ����Ԫ�أ�
��5�����Ǵ���ʹ�õ��ǺϽ�������Ϊ�Ͻ���и����������ܣ���ֱȴ�����Ӳ�ȴ�
�𰸣���1�����Ľ�����ǿ��ͭ��þ�Ľ�����ǿ��ͭ�����Ľ�����ǿ��ͭ�ȣ�
��2��þ�����ᷴӦ���ʿ죬��Ӧ���ң�Ѹ�ٲ����������ݡ�FeCl2+Mg=MgCl2+Fe��
��3���������⣬ͭ�������⡣����������Ͱװ������Һ�ȣ�
��4��������ʳ���к���������Ҫ����Ԫ�ء�
��5����

����Ŀ��ij��ѧ��ȤС���ͬѧ��������ѧҩƷ��ʱ��������һƿ��ǩ�������ɫ��Һ�������ǩ��ͼ��ʾ������ѯʵ������ʦ��֪����ƿ��ɫ��Һ��һ�ֳ��õ�����Һ��С��ͬѧ����ƿ��Һ����������̽����

������⣺��ƿ��ɫ��Һ��ʲô���ʵ���Һ��
��������裺С��ͬѧ��������¼���
��̼������Һ ����������Һ ���Ȼ�����Һ
���۽��� ����ʦ��ָ���£�С��ͬѧ�������ۣ���Ϊ��______�����費����������˵�������������ɣ�____________��
�������ϣ����ᱵ�Ȳ�����ˮ�ֲ��ܽ����̼������Һ�ʼ��ԣ�
Ba(OH)2�Ļ�ѧ������Ca(OH)2���ơ�
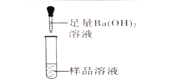
����ʵ�� С��ͬѧ��Ʋ�����������ʵ�飬��������С��ͬѧ�������������
��� | ʵ����� | ���ֵ���������� | ͬѧ����� |
1 |
| ������ɫ������ ��1��ͬѧ��Ϊ����ڳ��� | ��2��ͬѧ��Ϊ�˷������۲���ȷ������Ϊ�����������ᱵ��______��������ˮ |
2 |
| �Թ������������� ��2��ͬѧ��Ϊ����ڳ��� | ��3��ͬѧ��Ϊ�˷������۲���ȷ������Ϊ��������________________�� |
3 |
| ��Һ�����Ա仯�� ��3��ͬѧ��Ϊ����ڳ��� | ��1��ͬѧ��Ϊ�˷���������ȷ������Ϊʵ�����õ�ΰ���Թܾ��и�����ŵ����_______��дһ�����ɣ� |
ԭ������ �������ȷ��д����һ��ʵ��Ļ�ѧ����ʽ______
ʵ�鷴˼ ������������С��ͬѧ�ܽ���ȡ��ҩƷʱ����ע���������Ϊ�㵹Һ��ҩƷʱ��Ҫע��__________��