题目内容
【题目】如图是某反应的微观示意图.
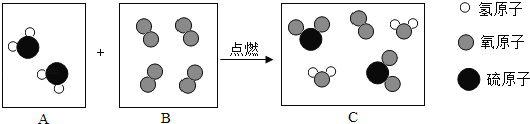
请回答:
(1)A框中的物质的化学式是________.
(2)B框中的物质属于_______(填序号).
①化合物 ②单质 ③纯净物 ④混合物
(3)此图说明化学反应前后发生改变的微粒是_______.
【答案】H2S; ②③ 分子
【解析】
(1)由反应的微观示意图可知,A框中物质的一个分子是由一个硫原子、两个氢原子构成的,故化学式是H2S;
(2)由反应的微观示意图可知,B框中的物质是氧气,氧气是由同种物质组成的,属于纯净物;氧气是由同种元素组成的纯净物,属于单质,故选②③;
(3)由反应的微观示意图可知,该反应前后分子的种类发生了改变,原子的种类不变,故此图说明化学反应前后发生改变的微粒是分子。

【题目】某校九年级“我们爱化学”活动小组的同学,在老师的指导下对稀硝酸的性质进行了实验探究。
(实验设计)(1)将紫色石蕊溶液滴入稀硝酸中,预计紫色石蕊溶液由紫色变为_____色;
(2)将铜片加入稀硝酸中,观察现象。
(实验验证)同学们按上述设计进行了实验,却发现紫色石蕊溶液变色后一会儿即褪去,铜片投入稀硝酸后,有气泡冒出,产生无色气体X,无色气体X遇空气变成红棕色有刺激性气味的气体。
(提出问题)(1)紫色石蕊溶液变色后为何会褪色?
(2)上述产生的无色气体X是什么?硝酸具有哪些特性?
(查阅资料)Ⅰ、硝酸具有强氧化性,可与Cu、Zn等多种金属反应生成相应的硝酸盐,但不会生成H2。
Ⅱ、某些气态含氮物质的物理性质如下表所示:
物质 | N2 | NH3 | NO | NO2 |
颜色 | 无色 | 无色 | 无色 | 红棕色 |
溶解性 | 不溶于水 | 极易溶于水 | 不溶于水 | 可溶于水 |
(猜想与分析)(1)小强同学认为紫色石蕊溶液变色后又褪色是由于试管不干净,含有其他杂质造成的,要证明小强的观点,应进行的操作是_____;
(2)大家一致认为红棕色气体是NO2,但对于无色气体X及变化的原因有不同的观点。
①小华同学认为气体X是N2,但遭到大家的一致反对,理由是_____;
②小明同学认为气体X是NH3,也遭到大家的一致反对,理由是_____;
③经讨论,最终大家获得了气体X是NO的共识。NO遇到空气中的氧气生成NO2的化学方程式为_____;
(表达交流)根据探究结果,请分析稀盐酸和铜不反应而稀硝酸却能与铜反应的原因:_____;
(反思拓展)(1)活动小组的同学对硝酸能与Zn反应很感兴趣,便取了一小块锌片投入稀硝酸中,发现锌片溶解,也出现上述Cu与稀硝酸反应的类似现象,确定生成了NO,并在老师的帮助下,测出恰好反应时Zn和HNO3的质量比为65:168,由此获得了Zn与稀硝酸反应的化学方程式为_____;
(2)活动小组的同学在老师的帮助下获得了一定质量分数的硝酸和锌反应对应的产物:质量分数为1%时生成NH4NO3;质量分数为15%时生成N2O;质量分数为50%时生成NO;质量分数为80%时生成NO2,由此可以得到的规律是_____;
(3)将铜片加入足量的浓硝酸中,发现反应后所得溶液呈绿色,活动小组的同学查阅资料得知,这是由于生成的红棕色NO2溶解在溶液中引起的,请设计一个简单的实验证明:_____。