题目内容
【题目】(8分)实验室常利用下图装置完成气体制备及性质实验。请回答:
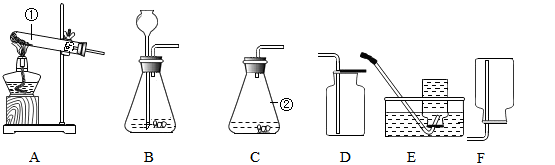
(1)指出编号仪器的名称:①_____________,②______________。
(2)若选择A和D装置制取氧气,反应的化学方程式为________________________,收集好的氧气瓶正方在桌面上,玻璃片光滑面朝_____(选“上”或“下” )。
(3)制取CO2时,选B装置比选C装置好的理由是___________________;用G装置来检验CO2,则G中的试剂为_______________。
(4)若要收集CO,选择的手机装置最好是_______________(填字母)。
【答案】(1)试管;锥形瓶;(2)2KMnO4 △ K2MnO4+ MnO2+ O2↑,上;
(3)控制反应速率;澄清石灰水
【解析】
试题分析:(1)仪器分别为:试管;锥形瓶;(2)根据图可知,应该是实验室用高锰酸钾来制取氧气,其化学方程式为:2KMnO4 △ K2MnO4+ MnO2+ O2↑,玻璃片光滑面应朝上,粗糙面与集气瓶接触;(3)图B能控制反应速率;检验二氧化碳用澄清石灰水

【题目】小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:
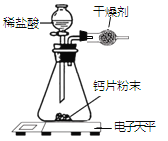
①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐 酸,置于电子天平上测出装置总质量。
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量。
③整理相关数据如下表,计算出钙片中碳酸钙的质量分数。
反应前总质量(克) | 275.58 |
反应后总质量(克) | 274.92 |
反应前后质量差(克) | 0.66 |
容器内气体质量差(克) | m |
(1)该实验中,对装置中的固态干燥剂的性质有何要求? 。
(2)反应前容器内是空气(密度为ρ1),反应后全部是CO2(密度为ρ2)。则反应前后容器(容积为V)内的气体质量差m为 。(用字母表示,反应物的体积忽略不计)
(3)小明查阅有关数据后,计算出反应前后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数。(CaCO3 + 2HCl = CaCl2 + H2O + CO2↑,钙片中的其它成分不与盐酸反应)


