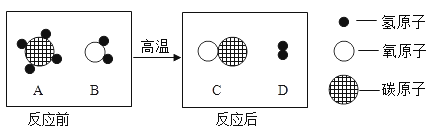
题目内容
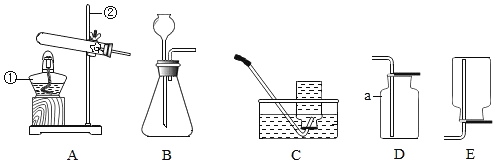
【题目】根据下列装置,回答问题:
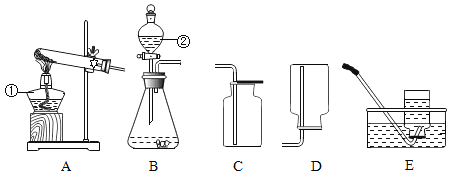
(1)写出图中标号仪器的名称:①___________;②___________。
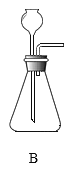
(2)实验室用稀盐酸和大理石制取二氧化碳时,发生反应的化学方程式为_________,反应的发生装置选用_____(填装置序号)。
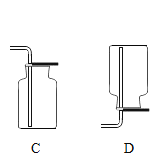
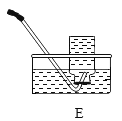
(3)通常状况下,氨气(NH3)是无色、有刺激性气味的气体,密度比空气小,极易溶于水。实验室通常用加热氯化铵和熟石灰固体混合物的方法制取氨气。实验室制取氨气的发生装置选用______________,收集装置选用_____________。
(4)实验室选择气体发生装置应考虑的因素是_________________________。
【答案】酒精灯 分液漏斗 CaCO3 +2HCl=CaCl2 +H2O +CO2↑ B A D 反应条件、反应物的状态
【解析】
(1)仪器的名称:①为酒精灯;②为分液漏斗。
(2)实验室中用大理石和稀盐酸反应来制取二氧化碳,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑,属于固液常温型,所以应该选择B装置来制取二氧化碳气体。
(2)实验室通常用加热氯化铵和熟石灰固体混合物的方法制取氨气,是两种固体加热制取,发生装置选A,氨气极易溶于水,不能用排水法收集,密度比空气小,可用向下排空气法收集。故选D。
(4)实验室选择气体发生装置应考虑的因素是反应条件、反应物的状态。

【题目】某化学兴趣小组的同学发现了一瓶露置于空气中的氢氧化钠溶液,他们对其成分展开了探究。
[提出问题]溶液的溶质是什么?
[建立假设]
(1)A 氢氧化钠 B 碳酸钠 C _________
(2)该兴趣小组的同学认为溶质可能是碳酸钠的理由是__________。
[设计实验]
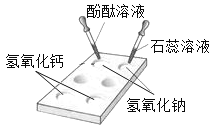
(3)小明的实验方案:取少量溶液,向其中滴加3滴酚酞溶液,溶液变为红色,小明立即得出结论溶质 是氢氧化钠;你认为小明的结论_______(填“正确”、“错误”或“无法确定”), 理由是_______________。
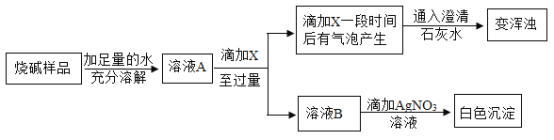
(4)小晶的实验方案:取少量溶液,向溶液中滴加稀盐酸,观察到溶液中出现大量_______________,小晶得出 结论溶质是碳酸钠。
(5)小明、小刚认为小晶的结论也是错误的,他们的理由是__________________。
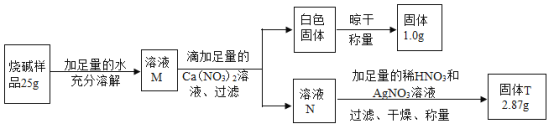
(6)大家交流讨论后修改的实验方案如下:
实验步骤 | 实验现象 | 解释、结论 |
取少量溶液,向溶液中加入过量的CaCl2溶液,过滤. | 有白色沉淀产生 | 反应的化学方程式为_______ |
取上述实验所得溶液少量,滴加3滴酚酞试剂. | 溶液变红 | C正确 |