题目内容
【题目】氧化亚铜(Cu2O)可用于生产船底防污漆,防止海生物对船舶设备的污损。现将Cu2O和Cu的固体混合物6.8g放入烧杯中,加入过量的质量分数为20%的稀硫酸30g,充分反应后,过滤、洗涤、干燥,得到4.8 g固体.已知:Cu2O+H2SO4=CuSO4+Cu+H2O
计算:
(1)硫酸是由_____种元素组成;
(2)硫酸中氢、硫、氧的原子个数比为_____;
(3)硫酸的相对分子质量为_____;
(4)原混合物中Cu2O与Cu的质量比____(写出过程,结果用最简整数比表示) .
【答案】三; 2:1:4 ; 98; 9:8.
【解析】
(1)硫酸由氢、硫、氧三种元素组成,故填三。
(2)硫酸的化学式为H2SO4,则硫酸中氢、硫、氧的原子个数比为2:1:4,故填2:1:4。
(3)硫酸的相对分子质量为1×2+32+16×4=98,故填98.
(4)解:设原混合物中Cu2O的足量为x

144:80=x:2g
x=3.6g
原混合物中Cu2O与Cu的质量比为3.6g:(6.8g3.6g)=9:8
答:原混合物中Cu2O与Cu的质量比为9:8。

 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案【题目】探究实验展示了化学的无穷魅力.我们在实验的过程中也提炼了许多探究方法.
(提出问题)小松想探究分子的运动速率与相对分子质量的关系.
(假设猜想)
①相对分子质量越大,分子运动速率越快.
②_____
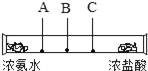
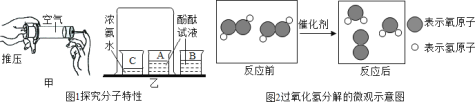
(查阅资料)已知浓氨水能挥发出氨气,浓盐酸能挥发出氯化氢气体,二者接触反应会产生白烟(氯化铵固体)
(设计实验)如图所示,在玻璃管两端分别放入蘸有浓氨水和浓盐酸的棉花团.
(实验现象)C处产生的白烟较多.
(解释与结论)氨分子的分子质量(相对分子质量)_____(填“大于”、“等于”或“小于”)氯化氢分子的分子质量(相对分子质量),由此可知,分子质量(相对分子质量)越_____(填“大”或“小”),分子的速率越_____(填“快”或“慢”).
(拓展探究)小松在完成上述实验后,还想研究分子运动速率与温度的关系.
他将等量的品红分别滴入到等量的热水和冷水中,其实验现象如下所示.
实验过程 | 冷水 | 热水 |
开始 | 红色扩散较慢 | 红色扩散较快 |
长久放置 | 最终均成为红色、均匀、透明的液体 | |
依据此实验现象,得出的结论是_____.