题目内容
【题目】I. 铜是生活中常见的金属,请回答下列问题:
(1)Cu 不活泼,通常情况下不与稀硫酸反应,但向 Cu 和稀硫酸的混合物中滴入 H2O2 后,溶液很快变蓝色,试写出该反应的化学方程式 __________________。
(2)将硫酸铜溶液和碳酸钠溶液混合,会析出 Cu2(OH)2CO3 绿色固体,试写出该反应的化学方程式______。
(3)火法炼铜的原理为:![]() ,下列说法中,正确的是 _______。
,下列说法中,正确的是 _______。
A Cu2S 只做还原剂
B O2 发生氧化反应
C S 元素被氧化
D 当 2 mol O2参加反应时,共转移了 10 mol 电子
II. 有一种固体混合物质 M,其中只可能含有 Na2CO3、NaNO3、Na2SO4、CuCl2、 BaCl2 中的一种或几种。请根据以下实验操作回答下列问题。
操作① 取少量 M 放入足量的水中充分搅拌、静置,得到白色沉淀和无色溶液,过滤。
操作② 向滤出的沉淀中加入足量稀硝酸,沉淀全部溶解,此时所得溶液仍为无色。
(1)M 中不能确定是否含有的物质是__________。
(2)上述实验过程中,发生反应的化学方程式为 ___________、 ________。
(3)向操作①后所得的无色溶液中滴加溶液 AgNO3溶液,一定能发生的反应的化学方程式为_____。
【答案】![]()
![]() C NaNO3
C NaNO3 ![]()
![]()
![]()
【解析】
(1)含铜离子的溶液为蓝色,Cu不活泼,通常情况下不与稀硫酸反应,但向Cu 和稀硫酸的混合物中滴入H2O2后,溶液很快变蓝色,根据质量守恒定律,该反应的化学方程式为:![]() 。
。
(2)将硫酸铜溶液和碳酸钠溶液混合,会析出 Cu2(OH)2CO3 绿色固体,根据质量守恒定律,该反应的化学方程式为:![]() 。
。
(3)A Cu2S中铜元素的化合价为+1,硫元素的化合价为-2,生成物中铜元素的化合价为0,硫元素的化合价为+4,所以Cu2S既是还原剂又是氧化剂,此选项错误;B O2中氧元素的化合价降低,氧气发生还原反应,此选项错误;C S元素的化合价升高,被氧化,此选项正确;D 当 2 mol O2参加反应时,共转移了8 mol 电子,此选项错误。故选C。
II. (1)取少量 M 放入足量的水中充分搅拌、静置,得到白色沉淀和无色溶液,由于含有铜离子的溶液为蓝色,碳酸铜是蓝色沉淀,故M 中无CuCl2。向滤出的沉淀中加入足量稀硝酸,沉淀全部溶解,此时所得溶液仍为无色。碳酸钡沉淀溶于稀硝酸,而硫酸钡沉淀不溶于稀硝酸,则M 中一定含有Na2CO3、BaCl2,无Na2SO4,不能确定是否含有的物质是NaNO3。(2)上述实验过程中,发生反应的化学方程式为:![]() 、
、![]() 。(3)由于M 中含有BaCl2、Na2CO3,发生了化学反应:BaCl2+Na2CO3=BaCO3↓+2NaCl,所以向操作①后所得的无色溶液中滴加溶液 AgNO3溶液,一定能发生的反应的化学方程式为
。(3)由于M 中含有BaCl2、Na2CO3,发生了化学反应:BaCl2+Na2CO3=BaCO3↓+2NaCl,所以向操作①后所得的无色溶液中滴加溶液 AgNO3溶液,一定能发生的反应的化学方程式为![]()

【题目】下列各组物质间不能通过一步反应就能实现如图转化的是( )
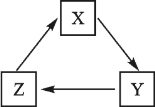
X | Y | Z | |
A | H2SO4 | HCl | H2O |
B | CuSO4 | CuCl2 | Cu(OH)2 |
C | CaCO3 | CO2 | K2CO3 |
D | Ca(OH)2 | NaOH | Mg(OH)2 |
A.AB.BC.CD.D