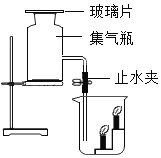
题目内容
【题目】某同学发现自己家菜园中的蔬菜生长迟缓,便施用了一种氮肥,下图是氮肥包装标签的部分文字,请回答下列问题。
xx牌化肥
主要点分:硝酸铵(NH4NO3)
净重:50kg/袋
含氮量:34.3%
(1)硝酸铵的相对分子质量为____________________。
(2)一袋化肥中氮元素的质量为____________千克?
(3)求一袋化肥中硝酸铵的质量____________。(写出第(2)、(3)题的计算过程)
【答案】80 17.15 49kg
【解析】
化合物的相对分子质量等于各原子的相对原子质量乘以原子个数之和。
(1)硝酸铵的化学式为NH4NO3,相对分子质量为![]() 。
。
(2)一袋化肥中氮元素的质量为 ![]()
(3)一袋化肥中硝酸铵的质量![]()

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】空气中氧气含量测定的再认识。
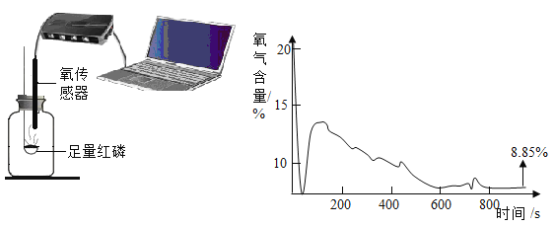
(一)某化学实验小组点燃红磷,并用氧传感器测定空气中的氧气含量并采集数据如上图。
(1)红磷在瓶中燃烧产生的现象是_____,红磷燃烧的化学方程式是_____。
(2)开始时氧气的含量持续下降,一方面是氧气被消耗,另一方面是生成物大量和氧传感器接触,但在110s时氧气的含量又有所上升,其可能原因是_____。
(3)从以上数据分析最终集气瓶中的氧气是否完全消耗_____。
(二)针对以上实验测定结果实验小组同学对该实验做了以下两种改进:

Ⅰ.根据铁在空气中生锈的原理设计如图实验装置,测定空气中氧气含量。
查资料:装置中饱和食盐水、活性炭会加速铁生锈。
测得实验数据如下表:
测量项目 | 实 验 前 | 实 验 后(冷却到室温后) | ||
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)的容积 | 导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 | 6.0 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式_____;该反应的基本类型是_____。
(2)根据上表数据计算,改进实验后测得的空气中氧气的体积分数是_____%(结果精确到0.1%)。
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:
①_____;②_____。
Ⅱ.将足量白磷放在集气瓶中,白磷能发生缓慢氧化从而消耗氧气,并用压强传感器测定瓶中压强的变化,根据压强的变化来计算空气中氧气的含量,实验装置及数据采集如下图。
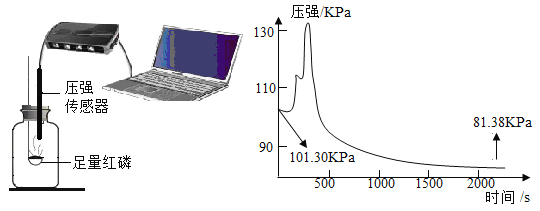
(1)在开始200s压强增大,增大的原因是_____。
(2)用上图所示数据计算用这种方法测得的空气中氧气的体积分数是_____%(结果精确到0.1%)。
(三)结论:测定空气中氧气含量用燃烧法测定结果误差较大,用缓慢氧化误差较小。
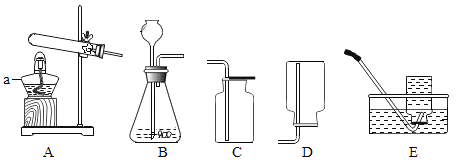
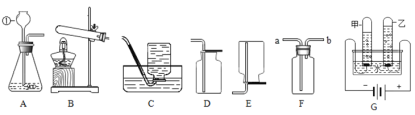
【题目】化学是一门以实验为基础的科学。请根据下列仪器和实验装置回答有关问题:
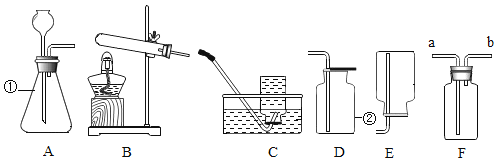
(1)写出标号仪器的名称:①________;②________;
(2)若选择高锰酸钾制取并收集较纯净的氧气,则应选择装置组合________(填字母),其反应的化学方程式是________________;
(3)用D装置收集氧气,验满的方法是________________________;
(4)若用F装置充满水来收集氧气,气体应从________(填a或b)端通入;
(5)某校兴趣小组取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
分析表中数据,完成下列问题:
①完全反应后,生成氧气的质量为________g;
②原混合物中氯酸钾的质量分数是多少?(精确到0.1%)________