题目内容
【题目】下列叙述正确的是( )
A.5gMg与3gO2反应可生成8gMgO
B.4gMg与4gO2反应可生成8gMgO
C.3.2gMg与4.8gO2反应可生成8gMgO
D.6gMg与4gO2反应可生成10gMgO
【答案】D
【解析】
镁在氧气中燃烧生成氧化镁,反应的化学方程式为2Mg+O2 2MgO,镁、氧气、氧化镁的质量比为
2MgO,镁、氧气、氧化镁的质量比为![]() 。
。
A、镁、氧气、氧化镁的质量比为![]() ,3gMg与2gO2反应可生成5gMgO,故A不正确;
,3gMg与2gO2反应可生成5gMgO,故A不正确;
B、镁、氧气、氧化镁的质量比为![]() ,6gMg与4gO2反应可生成10gMgO,故B不正确;
,6gMg与4gO2反应可生成10gMgO,故B不正确;
C、镁、氧气、氧化镁的质量比为![]() ,3.2gMgMg与2.4gO2反应可生成5.6gMgO,故C不正确;
,3.2gMgMg与2.4gO2反应可生成5.6gMgO,故C不正确;
D、镁、氧气、氧化镁的质量比为![]() ,6gMg与4gO2反应可生成10g生成10gMgO,故D正确。故选D。
,6gMg与4gO2反应可生成10g生成10gMgO,故D正确。故选D。

练习册系列答案
相关题目
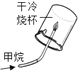
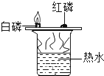
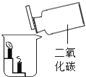
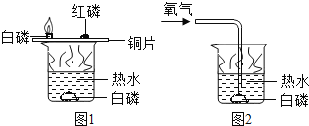
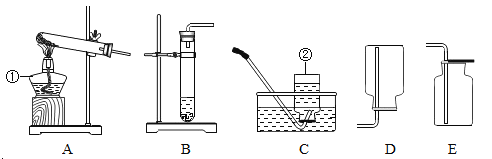
【题目】根据下图所示实验分析得出的结论中,不正确的是( )
|
|
|
|
A.甲烷燃烧生成二氧化碳和水 | B.铁能在氧气中燃烧 | C.白磷的着火点比红磷的低 | D.二氧化碳的密度比空气大,不燃烧也不支持燃烧 |
A. A B. B C. C D. D
【题目】把4g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示:
第一次 | 第二次 | 第三次 | |
氧气的质量(g) | 3 | 4 | 6 |
SO2的质量(g) | 6 |
请回答下列问题:
(1)写出此反应的化学方程式:_____;
(2)第一次实验中参加反应的硫、氧气和生成二氧化硫的质量之比是_____;
(3)通过计算,第二次实验生成二氧化硫的质量为_____;
(4)第三次生成的二氧化硫的质量为_____。