��Ŀ����
����Ŀ����4������������Ȼ��ص��ܽ��������ͼ��ʾ���ش��������⣺
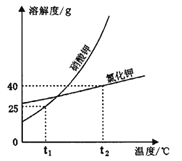
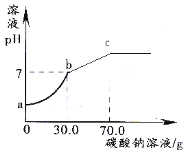
��1��t2��ʱ�������ʵĵ�����������Һ������t1�棬�������������ϴ���� ����Һ��
��2��t2��ʱ����50gˮ����ʢ��25g�Ȼ��ص��ձ��У�����ܽ�õ��Ȼ�����Һ�������� g�������¶Ȳ��䣬�����ձ����ټ���5gˮ����ֽ�����Ȼ�����Һ�����ʵ��������� �����������䡱��С������
��3����������л��������Ȼ���ʱ������ �����ᴿ�������
���𰸡���1������� ��2��70 ���� ��3����ȴ�ȱ�����Һ�������½ᾧ����
��������
����������ܽ�����¶�Ӱ�������ʣ���ͬ�ı�����Һ������ͬ���¶������ľ���࣬�ʣ�1��t2��ʱ�� �����ʵĵ�����������Һ������t1�棬�������������ϴ��������أ�(2�������Ȼ���t2��ʱ���ܽ�ȵ���ֵ��֪��50gˮ����ʢ��25g�Ȼ��ص��ձ��У�����ܽ�õ��Ȼ�����Һ��������70g�������ձ����ټ���5gˮ����ֽ�����Ȼ�����Һ�����ʵ������������䣬��Ϊ�ڼ�ˮ֮ǰ��Һ������������ʣ�࣬����ˮ�����ܽ���ʣ������ʣ���ȻΪ������Һ���������ʵ������������䡣��3����Ϊ����ص��ܽ�����¶ȵ����߶��������ʵõ�����ز��ý��½ᾧ��