题目内容
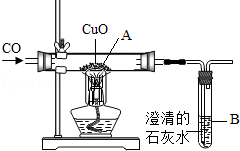
下面是某兴趣小组同学做的2个小实验。根据实验内容回答下列问题(仪器的固定装置已经省略)。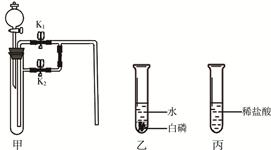
(1)若甲中盛有二氧化锰,连接甲乙装置,关闭K1打开K2,从分液漏斗向甲中加入适量双氧水,关闭分液漏斗活塞,观察到乙中导管口有气泡冒出,白磷不燃烧;关闭K2打开K1,则乙中的现象是 ,且白磷燃烧。
①甲中发生反应的化学方程式是 。
②实验过程中,白磷产生现象差异的原因是 。
(2)若甲中充满二氧化碳(K1、K2关闭),连接甲丙,从分液漏斗向甲中加入适量的澄清石灰水,关闭分液漏斗活塞,一段时间后,打开K1,整个实验过程中观察到甲中的现象是 。
(1)液面上升 ①2H2O2 2H2O + O2↑
2H2O + O2↑
②甲中液体被压入乙中,过氧化氢发生分解反应放热,使乙中温度达到白磷的着火点
(2)甲中石灰水变浑浊,打开K1后,丙中液体流入甲中,有气泡产生,溶液由浑浊逐渐变澄清(2分,答不全不得分)
解析

二十一世纪是海洋开发与利用的世纪,我市规划确立了“蓝色经济”发展战略,海洋化学资源的综合利用将是重点发展领域之一。以下是某研究性学习小组在探究海水综合利用中遇到的问题,请你参与解决并填空:
问题一、海水制镁过程中如何富集镁离子?
甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳。
乙:高温加热蒸发海水后,加入石灰乳。
丙:向晒盐后的卤水中,加入石灰乳。
通过分析比较,你认为 ① 的设想最为经济合理(选填“甲”、“乙”或“丙”)。
问题二、粗盐纯化过程中如何除去可溶性杂质?
粗盐中含有硫酸钠、氯化钙等杂质。提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是完全除尽硫酸钠;再加过量的碳酸钠溶液,除去杂质阳离子;滤去沉淀,向滤液中加入 ② ,将溶液的pH调为7,即得到精盐水。
问题三、海水“制碱” 的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中含有碳酸钠和氢氧化钠;
丙的猜想:样品中只含有氢氧化钠。
他们做出上述三种猜想的科学依据是 ③ 。
【实验、记录与分析】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全 溶液,再加入过量 ④ | 生成白色沉淀 | 丙的猜想 不成立 |
| 2 | 取步骤1反应后的溶液于试管中 ⑤ | ⑥ | 只有甲的 猜想成立 |
小芳同学从超市购买了一瓶维生素C泡腾片。下图是标签上的部分内容。
| 维生素C泡腾片 功能:补充人体维生素C,增强机体抵抗力 主要成分:维生素C 辅料成分:碳酸氢钠、氯化钠、酒石酸晶体、蔗糖、糖精钠、阿朴胡萝卜醛、橘味香精、橙味香精、维生素B 贮藏:低温、避光、防潮 |
小芳同学根据使用说明将维生素C泡腾片放入一杯水中,发现维生素C泡腾片逐渐溶解,产生大量气泡,片刻后变为一杯鲜甜的橙味饮品。小芳同学感到很好奇,产生的气泡是什么呢?
请你参与小芳同学的探究:
【提出问题】维生素C泡腾片放入水中,产生的气泡是什么呢?
【我的猜想】气体成分是________,理由是_________________________。
【实验方案】
| 实验步骤 | 实验现象 | 实验结论 |
| 将一片维生素C泡腾片放入水中,将产生的气体通入__ __________________ | | |
根据维生素C泡腾片储存条件,请说明保存时要低温和防潮的原因是:
①______________________________________________________;
②______________________________________________________。
某化学兴趣小组的同学对一瓶久置的熟石灰粉末的组成进行实验探究,请你一起参与他们的探究活动。
[提出问题]这瓶熟石灰粉末是否已经变质生成了CaCO3?
[进行猜想]猜想一: 。
猜想二:熟石灰部分变成了CaCO3。
猜想三:熟石灰没有变质。
[设计实验]该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表中相关实验内容。
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样,加适量水,搅拌,过滤 ②取少量滤液于试管中,滴入酚酞试液 ③取少量滤渣于试管中,加入盐酸 | ②无明显变化。 ③ 。 | 猜想一成立 |
[反思与应用]①要证明猜想二成立,可参照上述实验方案进行探究,在步骤②中产生的实验现象是 。
②熟石灰变质的化学反应方程式为 ,因此实验室中应 保存。
[数据处理]将10g已经全部变质的熟石灰粉末(即CaCO3)放入烧杯中,加入一定量的稀盐酸,恰好完全反应,产生气体,完全反应后所得溶液质量为55.6g。
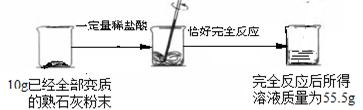
计算:①生成气体的质量为 g ;参与反应的HCl的质量为 g;
②反应前稀盐酸中溶质的质量分数。(写出计算过程,结果精确到0.1%)
某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应)。已知:浓硫酸可作为干燥剂;草酸晶体(H2C2O4·2H2O )的性质见下表:
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |

(2)图 2 是验证热分解产物中含 CO 、 CO2的装置。
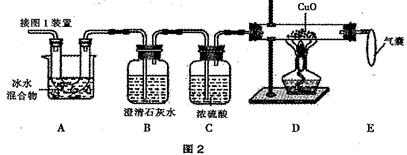
① 装置 A 的作用是_____________________,气囊的作用是_____________________。
② 证明存在 CO2的现象是______________,证明存在 CO 的现象是______________。
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:_________________________________________________。