题目内容
根据图1回答问题.
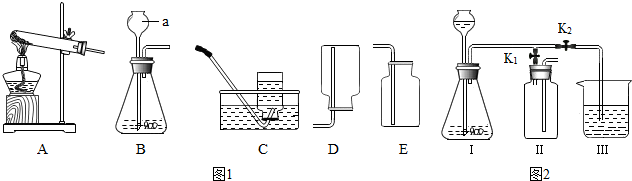
(1)甲同学将所学气体制取的知识整理如下,请你帮助他完成相关内容.
①出图1中有标号仪器的名称:a .
②用双氧水和二氧化锰来制取氧气时,可选用的发生装置是 (填序号,下同),可选用装置 收集氧气,化学方程式是 .③反应结束后,欲将二氧化锰回收再利用应进行的主要操作是 .
③写出高锰酸钾法制氧气的方程式
④实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置是 .
(2)乙同学设计的实验装置(如图2),既可用于制取气体,又可用于探究物质性质.
①当打开K1、关闭K2时,利用I、Ⅱ装置可进行的实验是 (填序号).a.大理石与稀盐酸反应制取二氧化碳 b.锌与稀硫酸反应制取氢气
②当打开K2、关闭K1,利用I、Ⅲ装置可以检验生成的二氧化碳,反应的化学方程式为 ;若要证明二氧化碳与水发生反应,烧杯中应放入的试剂是 .

(1)甲同学将所学气体制取的知识整理如下,请你帮助他完成相关内容.
①出图1中有标号仪器的名称:a
②用双氧水和二氧化锰来制取氧气时,可选用的发生装置是
③写出高锰酸钾法制氧气的方程式
④实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置是
(2)乙同学设计的实验装置(如图2),既可用于制取气体,又可用于探究物质性质.
①当打开K1、关闭K2时,利用I、Ⅱ装置可进行的实验是
②当打开K2、关闭K1,利用I、Ⅲ装置可以检验生成的二氧化碳,反应的化学方程式为
考点:常用气体的发生装置和收集装置与选取方法,混合物的分离方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的检验和验满,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),因此需要加热.当打开K1、关闭K2时,利用I、Ⅱ装置可进行的实验是:锌与稀硫酸反应制取氢气,因为进气管短,氢气的密度比空气的密度小;当打开K2、关闭K1,利用I、Ⅲ装置可以检验生成的二氧化碳,二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;若要证明二氧化碳与水发生反应,烧杯中应放入的试剂是:紫色石蕊试液,会发现紫色变红色.
解答:解:(1)长颈漏斗方便加液体药品,如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;二氧化锰不溶于水,因此可以用过滤的方法分离;如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),因此需要加热;故答案为:①长颈漏斗;②B;C或E;2H2O2
2H2O+O2↑;过滤;③2KMnO4
K2MnO4+MnO2+O2↑;④A;
(2)当打开K1、关闭K2时,利用I、Ⅱ装置可进行的实验是:锌与稀硫酸反应制取氢气,因为进气管短,氢气的密度比空气的密度小;当打开K2、关闭K1,利用I、Ⅲ装置可以检验生成的二氧化碳,二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;若要证明二氧化碳与水发生反应,烧杯中应放入的试剂是:紫色石蕊试液,会发现紫色变红色;故答案为:①b;②Ca(OH)2+CO2=CaCO3↓+H2O;紫色石蕊试液;
| ||
| ||
(2)当打开K1、关闭K2时,利用I、Ⅱ装置可进行的实验是:锌与稀硫酸反应制取氢气,因为进气管短,氢气的密度比空气的密度小;当打开K2、关闭K1,利用I、Ⅲ装置可以检验生成的二氧化碳,二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;若要证明二氧化碳与水发生反应,烧杯中应放入的试剂是:紫色石蕊试液,会发现紫色变红色;故答案为:①b;②Ca(OH)2+CO2=CaCO3↓+H2O;紫色石蕊试液;
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的检验等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
在化学反应4NH3+5O2
4X+6H2O中,X的化学式为( )
| ||
| △ |
| A、N2O5 |
| B、NO2 |
| C、NO |
| D、HNO3 |
下列物质是由分子构成的是( )
| A、铁 | B、氢气 | C、氯化钠 | D、铜 |
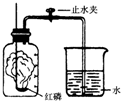 用如图装置测量空气中氧气的含量.弹簧夹夹乳胶管,点燃燃烧匙内的红磷立即伸入集气瓶并将塞子塞紧.回答下列问题:
用如图装置测量空气中氧气的含量.弹簧夹夹乳胶管,点燃燃烧匙内的红磷立即伸入集气瓶并将塞子塞紧.回答下列问题: