题目内容
实验室制取氢气的残留液中含有硫酸锌和剩余的硫酸,从环境保护和资源利用的角度都要求对硫酸锌加以回收和利用.
(1)现有下列试剂:①NaOH溶液 ②Na2CO3粉末 ③CaO粉末 ④ZnO粉末(难溶于水),欲除去残留液中的硫酸可选用的理想试剂为 (填编号),其反应的化学方程式 .
(2)欲从第一步操作(加入的试剂过量)后的混合液中获得硫酸锌固体(ZnSO4),则应选择的操作是 (请按操作顺序填编号).
A.洗涤 B.过滤 C.蒸发 D.烘干.
(1)现有下列试剂:①NaOH溶液 ②Na2CO3粉末 ③CaO粉末 ④ZnO粉末(难溶于水),欲除去残留液中的硫酸可选用的理想试剂为
(2)欲从第一步操作(加入的试剂过量)后的混合液中获得硫酸锌固体(ZnSO4),则应选择的操作是
A.洗涤 B.过滤 C.蒸发 D.烘干.
考点:酸、碱性废水的处理,蒸发与蒸馏操作,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:化学与环境保护
分析:根据氧化锌与硫酸反应,且不生成新的杂质;充分反应后过滤,将滤液蒸发、冷却、结晶,即可得到较纯净的硫酸锌晶体进行解答.
解答:解:NaOH溶液不仅能和硫酸反应,生成新的杂质硫酸钠,而且能和硫酸锌反应,故不能使用;
Na2CO3粉末不仅能和硫酸反应,生成新的杂质硫酸钠,而且能和硫酸锌反应,故不能使用;
CaO粉末能和硫酸反应,生成新的杂质硫酸钙,故不能使用;
氧化锌与硫酸反应生成了硫酸锌和水,反应的化学方程式:ZnO+H2S04═ZnS04+H20,不生成新的杂质;硫酸完毕,氧化锌粉剩余,充分反应后过滤,然后将滤液蒸发、冷却、结晶,即可得到较纯净的硫酸锌晶体;
故答案为:(1)④,ZnO+H2S04═ZnS04+H20;(2)BC
Na2CO3粉末不仅能和硫酸反应,生成新的杂质硫酸钠,而且能和硫酸锌反应,故不能使用;
CaO粉末能和硫酸反应,生成新的杂质硫酸钙,故不能使用;
氧化锌与硫酸反应生成了硫酸锌和水,反应的化学方程式:ZnO+H2S04═ZnS04+H20,不生成新的杂质;硫酸完毕,氧化锌粉剩余,充分反应后过滤,然后将滤液蒸发、冷却、结晶,即可得到较纯净的硫酸锌晶体;
故答案为:(1)④,ZnO+H2S04═ZnS04+H20;(2)BC
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
下列说法错误的是( )
| A、原子呈电中性 |
| B、原子核一定含有中子 |
| C、原子核一定含有质子 |
| D、单质中只含一种元素 |
有关使用酒精灯的叙述正确的是( )
| A、给物质加热时,应该用酒精灯的外焰 |
| B、酒精灯的内焰温度最高 |
| C、点燃酒精灯时,应把灯帽倒置在桌子上 |
| D、点燃另一个酒精灯时,可以对火 |

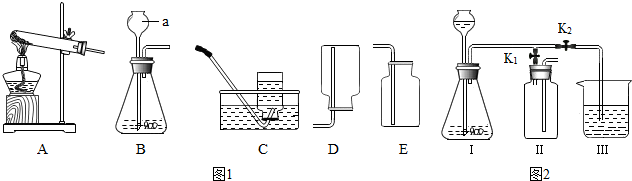
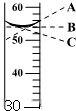 “由生活走进化学,从化学走向社会.”请回答下列问题:
“由生活走进化学,从化学走向社会.”请回答下列问题: 家庭小实验是化学学习的有益拓展.在实验中我们可以选用生活用品来代替一些化学仪器,如眼药水瓶可以代替胶头滴管,吸管可以代替导气管等.现有一医用注射器,请你思考它可以代替哪些常用仪器?请举出四种.
家庭小实验是化学学习的有益拓展.在实验中我们可以选用生活用品来代替一些化学仪器,如眼药水瓶可以代替胶头滴管,吸管可以代替导气管等.现有一医用注射器,请你思考它可以代替哪些常用仪器?请举出四种.