题目内容
【题目】根据如图提供的几种物质的溶解度曲线,判断下列说法正确的是( ) 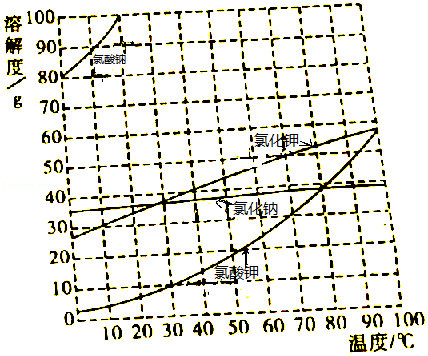
A.氯酸钾中混有少量氯化钠,提纯氯酸钾最好用蒸发结晶的方法
B.30℃氯酸钾饱和溶液的溶质质量分数为10%
C.80℃时7gNaCl和20g水能形成饱和溶液
D.控制温度,图中氯酸钠和氯化钾能发生化学反应
【答案】D
【解析】解:A、氯酸钾的溶解度受温度变化影响较大,所以氯酸钾中混有少量氯化钠,提纯氯酸钾最好用降温结晶的方法,故A错误; B、30℃时,氯酸钾的溶解度是10g,所以氯酸钾饱和溶液的溶质质量分数为: ![]() ×100%=9.1%,故B错误;
×100%=9.1%,故B错误;
C、80℃时,氯化钠的溶解度是40g,所以7gNaCl和20g水不能形成饱和溶液,故C错误;
D、氯酸钠和氯化钾交换成分可以得到氯酸钾和氯化钠,控制温度在10﹣30℃之间,氯化钠的溶解度较大,氯酸钾的溶解度较小,会以晶体形式析出,所以图中氯酸钠和氯化钾能发生化学反应,故D正确.
故选:D.
【考点精析】利用结晶的原理、方法及其应用和固体溶解度曲线及其作用对题目进行判断即可得到答案,需要熟知结晶的两种方法:蒸发溶剂,如NaCl(海水晒盐)和降低温度(冷却热的饱和溶液,如KNO3);1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

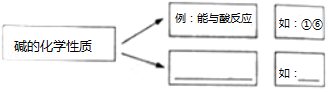
【题目】物质的性质决定用途.下列是物质的一些性质:①密度小,很稳定、②有吸附性、③有导电性、④易升华、⑤能与酸反应.请选择恰当的数字序号填空.
用途 |
|
|
|
|
|
性质 | (1)石墨 | (2)活性炭 | (3)氦气 | (4)碳酸氢钠 | (5)干冰 |
【题目】常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌,如图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见表).下列实验与图象对应关系合理的是( )
M | N | y | |
A | 水 | 氧化钙 | 溶液的温度 |
B | 水 | 氢氧化钠 | 溶液的pH |
C | 饱和氯化钠溶液 | 氯化钠 | 溶液的溶质质量分数 |
D | 硫酸铜溶液 | 铁粉 | 溶液的质量 |

A.A
B.B
C.C
D.D