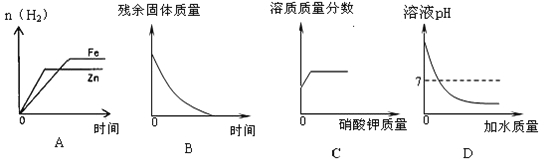
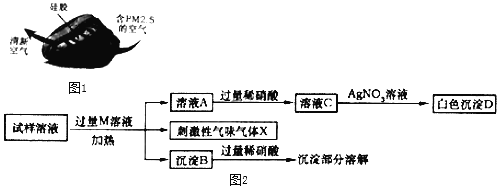
题目内容
【题目】根据下图所示的实验装置回答问题。
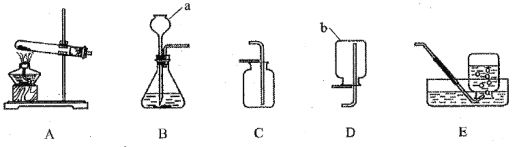
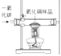
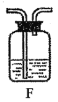
(1)写出标注仪器的名称:a_______,b_______。
(2)实验室用A装置制取氧气,试管内的暗紫色固体是___________(填名称)。写出实验室用B装置制取氧气的化学方程式_____________。选择E装置收集氧气,当看到_______,说明气体收集满了。
(3)实验室制取二氧化碳选用的发生装置是____________(填字母代号),反应的化学方程式为______________________。
(4)用F装置除去二氧化碳气体中的少量水蒸气,F中放入的试剂是____________。
【答案】 长颈漏斗 集气瓶 高锰酸钾 2H2O2MnO22H2O+O2↑ 集气瓶口有气泡向外冒出 B CaCO3+2HCI==CaCl2 +H2O十CO2↑ 浓硫酸(或浓H2SO4溶液)
【解析】(1)根据常见仪器解答;(2)根据A装置试管口装有棉花,适宜加热分解高锰酸钾制取氧气解答;B装置属于固液混合常温型发生装置,适宜分解过氧化氢溶液制取氧气;根据用排水法收集氧气验满的方法解答;(3)根据碳酸钙与稀盐酸在常温下反应生成氯化钙、水和二氧化碳解答;(4)根据浓硫酸有吸水性解答。(1)标注仪器的名称:a长颈漏斗,b集气瓶;(2) A装置试管口装有棉花,适宜加热分解高锰酸钾制取氧气,故试管内的暗紫色固体是高锰酸钾;
B装置属于固液混合常温型发生装置,适宜过氧化氢溶液在二氧化锰的催化下分解生成水和氧气,反应的化学方程式为2H2O2MnO22H2O+O2↑;选择E装置收集氧气,当看到集气瓶口有气泡向外冒出,说明气体收集满了;(3) 碳酸钙与稀盐酸在常温下反应生成氯化钙、水和二氧化碳,反应物是固体与液体,反应在常温下进行,故实验室制取二氧化碳选用的发生装置是B,反应的化学方程式为CaCO3+2HCl=CaCl2 +H2O+CO2↑;(4)用F装置除去二氧化碳气体中的少量水蒸气,F中放入的试剂是浓硫酸(或浓H2SO4溶液)。

【题目】下列实验设计不能达到实验目的是( )
选项 | A | B | C | D |
实验目的 | 除去CO中的CO2,并回收CO | 探究可燃物燃烧所需的条件 | 除去氧化铜粉末中的铜粉 | 鉴别NH4NO3、CuSO4和NaCl三种白色粉末 |
实验设计 |
|
|
|
|
A. A B. B C. C D. D
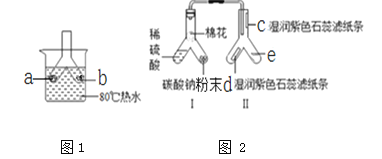
【题目】氧化铜能与多种物质反应,能否与氨气(NH3)反应呢?在老师的指导下,某同学进行了探究。(注:无水硫酸铜遇水变蓝)
(实验设计)按图设计组装好仪器,检查气密性,装入药品。
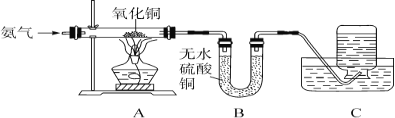
(进行实验)
(1)A中氧化铜全部转化成光亮的红色固体。
(2)B中U形管内物质变蓝。
(3)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是___________________。
(4)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞溶液,溶液呈________色,原因是______________。
(实验结论)氧化铜和氨气发生反应,化学方程式是_______________________。
(继续探究)
(1)测得有关数据如下表:
质量 | 实验前 | 实验后 |
氧化铜粉末+玻璃管 | 65.6g | 59.2g |
在此反应中,参加反应的氧化铜的质量为________g。
(2)A中玻璃管内的反应证明,氨气的化学性质与____________(填物质化学式)有相似之处。