题目内容
【题目】A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是( )
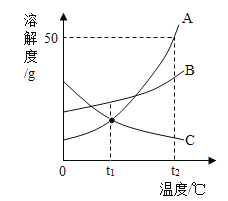
A. t1℃时,A、C两种物质的饱和溶液中溶质的质量相等
B. 将A,B、C三种物质的饱和溶液变为不饱和溶液,可采用升温的方法
C. 将 t2℃时A、B、C三种物质的饱和溶液降温至 t1℃,所得溶液的溶质质量分数的大小关系是B>C=A
D. t2℃时,把A、B、C三种物质各25g分别入50g水中均得到饱和溶液,但溶质和溶剂的质量比不相等
【答案】D
【解析】
根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
A、t1℃时,A,C两种物质的溶解度相等,但是饱和溶液的质量不能确定,所以饱和溶液中溶质的质量不能确定,此选项错误;
B、A、B两种物质的溶解度随温度的升高而增大,将A、B两种物质的饱和溶液变为不饱和溶液,可采用升温的方法,C物质的溶解度随温度的升高而减小,饱和溶液变为不饱和溶液,可采用降温的方法,此选项错误;
C、降低温度,A、B两种物质的溶解度减小,t1℃时,B物质的溶解度大于A,则将 t2℃时A、B两种物质的饱和溶液降温至 t1℃,所得溶液的溶质质量分数的大小关系是B>A。降低温度,C物质的溶解度增大,应该按照 t2℃时的溶解度计算, t2℃时C的溶解度小于t1℃A的溶解度,故所得溶液的溶质质量分数的大小关系是B>A>C,此选项错误;
D、t2℃时,A物质的溶解度是50g,B、C物质的溶解度小于50g。所以把A、B、C三种物质各25g分别入50g水中均得到饱和溶液,但溶质的质量不相等,所以溶质和溶剂的质量比不相等,此选项正确。
故选:D。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案