题目内容
【题目】治理污染、保护环境,事关人民群众的身体健康和社会的可持续发展。
(1)下列环境问题与燃煤有直接关系的是_____(填序号)。
A酸雨 B温室效应 C可吸入颗粒物增加
(2)烟气脱硫是目前控制燃煤的重要途径。如钠碱循环法是利用亚硫酸钠(Na2SO3)溶液脱除烟气中的SO2,生成亚硫酸氢钠(NaHSO3),反应的化学方程式为_____,Na2SO3可由NaOH溶液吸收SO2制得,反应的化学方程式为_____。
(3)大气中CO2含量不断升高,使全球气候问题日趋严重。科学家们正在努力尝试通过多种途径减少CO2的排放或将CO2转化为有用物质。
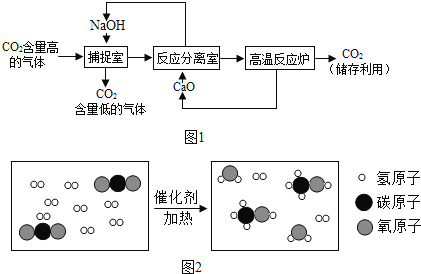
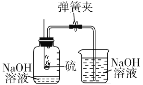
①途径一:利用NaOH溶液来“捕捉”CO2,并将CO2储存或利用,流程如图。
下列有关该过程的叙述正确的是_____;(填序号)
A该过程可实现CO2零排放
B该过程只有2种物质可以循环利用
C反应分离室中分离物质的操作是蒸发、结晶
D该过程至少发生了4个化学反应
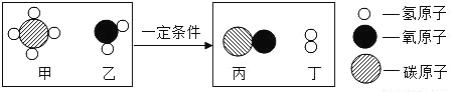
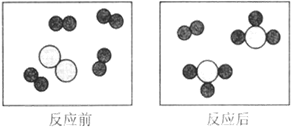
②途径二:将CO2转化为甲醇(CH3OH),其反应的微观过程如图2所示,上述反应的化学方程式为_____。
【答案】ABC Na2SO3+SO2+H2O═2NaHSO3 2NaOH+SO2═Na2SO3+H2O BD CO2+3H2 CH3OH+H2O
CH3OH+H2O
【解析】
(1)将煤燃烧能生成二氧化碳、二氧化硫等物质,还能产生大量的灰尘,生成的二氧化碳能形成温室效应,生成的二氧化硫能形成酸雨,产生的大量灰尘增加了空气中的可吸入颗粒物;故选:ABC;
(2)利用亚硫酸钠(Na2SO3)溶液脱除烟气中的SO2,生成亚硫酸氢钠(NaHSO3),反应的化学方程式为:Na2SO3+SO2+H2O═2NaHSO3;
Na2SO3可由NaOH溶液吸收SO2制得,反应的化学方程式为2NaOH+SO2═Na2SO3+H2O;
(3)①根据题干提供的信息进行分析,碳酸钙高温能分解生成氧化钙和二氧化碳;增大反应物的接触面积能促进反应的进行;氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠;而氢氧化钠溶液可来“捕捉”CO2;故该过程只有碳酸钙、氢氧化钠等都可以循环利用;
而含有二氧化碳含量低的气体排出,并没有“实现CO2零排放”;
在“反应室“中发生的反应有CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,所以分离CaCO3和NaOH用过滤操作;
该过程化学反应有:碳酸钙高温能分解生成氧化钙和二氧化碳、氧化钙能与水反应生成氢氧化钙、氢氧化钠溶液与二氧化碳反应、氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故至少发生了4个。
②根据微观示意图可知:CO2和H2在条件下转化为甲醇(CH3OH)和水,配平即可,故其化学方程式为:CO2+3H2 CH3OH+H2O;
CH3OH+H2O;
答案:
(1)ABC;
(2)Na2SO3+SO2+H2O═2NaHSO3;2NaOH+SO2═Na2SO3+H2O;
(3)①BD;②CO2+3H2 CH3OH+H2O
CH3OH+H2O