题目内容
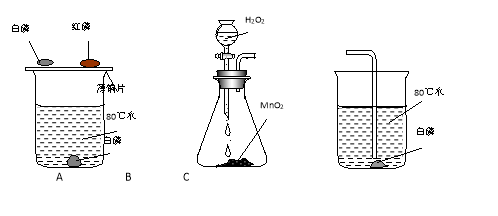
【题目】实验室利用下图装置制取氧气,并检验氧气的性质。
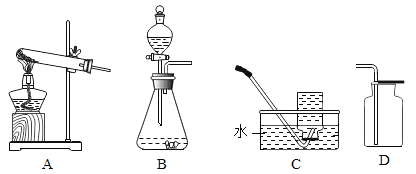
①A中盛放固体的仪器名称为_____;A装置制取氧气,反应的化学方程式为_______________。
②“C”的收集方法称为________;铁丝在氧气中燃烧的现象为_____,反应的化学方程式为_____。
③B中锥形瓶中放入的二氧化锰的作用是_______,B装置中使用分液漏斗不使用长颈漏斗的原因是_______
【答案】试管 2KClO3![]() 2KCl+3O2↑ 排水集气法 火星四射,放出大量的热,生成黑色固体 3Fe+2O2
2KCl+3O2↑ 排水集气法 火星四射,放出大量的热,生成黑色固体 3Fe+2O2![]() Fe3O4 催化作用 分液漏斗可以控制液体的滴加速度,获得平稳气流。
Fe3O4 催化作用 分液漏斗可以控制液体的滴加速度,获得平稳气流。
【解析】
①A 中盛放固体的仪器名称为试管;实验室用A装置制取氧气,属于固体加热型,试管口没有放一团棉花,是采用的加热氯酸钾和二氧化锰混合物的方法,氯酸钾在二氧化锰的催化作用下、在加热条件下生成氯化钾和氧气,反应的化学方程式为:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
②“C”的收集方法称为排水法;铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体;铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为3Fe+2O2![]() Fe3O4;③B 属于固—液常温型发生装置,采用的分解过氧化氢溶液的方法,放入的二氧化锰的作用是起催化作用。B 装置中使用分液漏斗不使用长颈漏斗的原因是能控制滴加液体的速率,从而控制反应的速率,获得平稳气流。
Fe3O4;③B 属于固—液常温型发生装置,采用的分解过氧化氢溶液的方法,放入的二氧化锰的作用是起催化作用。B 装置中使用分液漏斗不使用长颈漏斗的原因是能控制滴加液体的速率,从而控制反应的速率,获得平稳气流。

 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案【题目】多角度地认识溶液,有助于我们更好地了解其在生产生活中的重要作用。
(1)将生石灰与足量的水混合,充分搅拌后静置。上层清液为澄清石灰水,属于_______________;下层未完全溶液的部分未石灰乳,属于_______________。
A溶液 B悬浊液 C乳浊液
(2)不能用于说明![]() ,溶液是均一、稳定的是____________。
,溶液是均一、稳定的是____________。
A溶液各部分颜色相同 B溶液各部分溶质质量分数相同
C溶液久置后颜色不变 D滴入![]() 溶液有蓝色沉淀生成
溶液有蓝色沉淀生成
(3)将一定量的下列物质分别投入到100g水中充分溶解,计算所得溶液的溶质质量分数。
物质名称 | 投入质量 |
| 溶质质量分数 |
氯化钠 |
|
| _____ |
硝酸钾 |
|
| _____ |
胆矾 |
|
| _____ |
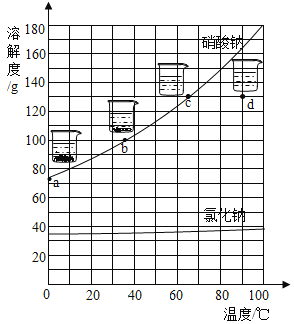
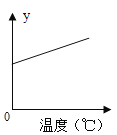
(4)20℃时,某物质在不同质量的水中溶解达到饱和时,溶质的质量与水的质量关系如图所示。
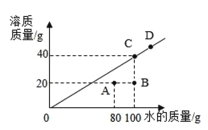
①![]() 时,该物质的溶解度是__________________溶质。
时,该物质的溶解度是__________________溶质。
②若D点对应的是120g水,则溶质质量为____________g
③如图可知溶液A点转变成B点状态,可通过增加溶剂(加20g水)的方式实现。则溶液从B点转变成C点状态,可通过_____________方式实现;