题目内容
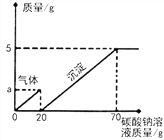
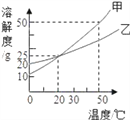
【题目】如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
A. 甲的溶解度大于乙的溶解度
B. 20℃时,甲、乙的饱和溶液中溶质与溶液的质量比为1:4
C. 将50℃甲物质的饱和溶液降温到30℃时,溶液质量减小
D. 将甲、乙两种物质的溶液分别从50℃降温至20℃时,溶液中溶质质量分数均为25%
【答案】C
【解析】A、没有指定温度,无法比较溶解度,错误;B、由溶解度曲线可知,20℃时,甲、乙的溶解度相等为25g,即100g溶剂中最多溶解25g溶质。因此20℃时,甲、乙的饱和溶液中溶质与溶液的质量比为25g:(25g+100g)=1:5,错误;C、由溶解度曲线可知,甲的溶解度随温度的升高而增大,故将50℃甲物质的饱和溶液降温到30℃时,有甲晶体析出,溶液质量减小,正确;D、50℃时,甲、乙两种物质的溶液是否饱和不确定,故将甲、乙两种物质的溶液分别从50℃降温至20℃时,溶液中溶质质量分数无法确定,错误。故选C。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案【题目】溶液在生产、生活中起着十分重要的作用。
(1)可作为溶质的是_______。
A.只有固体 B. 只有液体
C.只有气体 D. 气体、液体、固体都可以
(2)物质加入足量水中,能形成无色透明溶液的是_______。
A.汽油 B. 面粉 C. 纯碱 D. 硫酸铜
(3)物质加入水中形成溶液过程中,温度会升高的是_______。
A.烧碱 B. 氯化钠 D. 氧化钙 D. 碳酸钙
(4)下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度g/100g水 | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
①两种物质中,溶解度受温度影响变化较大的是__________。
②NaCl和KNO3溶解度相等的温度范围是__________。
③KNO3晶体中含有少量NaCl,提纯KNO3晶体的方法是__________。
④60℃时,按图示操作:
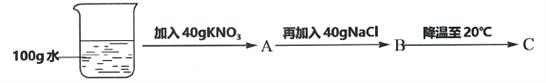
A中溶液是__________(填“饱和”或“不饱和”)溶液,C中溶液的总质量是__________g。
⑤50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液__________(填“大于”“等于”或“小于”)KNO3溶液。
【题目】(8分)在日常生活中,我们发现切过咸菜的刀更容易生锈.而除锈用稀盐酸比稀硫酸快。为了进一步验证上述现象,某校师生做了以下相关分组实验,请你根据自己平时课堂学习的体验一起参与讨论并回答相关问题。
(步骤一)未打磨的铝片浸入氯化铜溶液中,迅速产生大量气泡和疏松的紫红色固体,并放热,片刻后溶液由蓝绿色变成无色。
(1)若要正视紫红色固体中是否含有氧化铜,可用 ▲ 溶液(填一试剂)加以检验。
(步骤二)未打磨的铝片浸入硫酸铜溶液中,一段时间内没有明显现象。
(2)比较步骤一、二,你能得出的结论是: ▲ 。
(步骤三)打磨过的铝片浸入硫酸铜溶液中,其操作、现象和结论见下表。
(3)试将“影响因素”选项前恰当的字母序号填入答题卡指定位置。
实验操作 | 使用现象 | 对比结论 |
Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出。 | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体。 | 现象一与现象二对比,说明 |
现象二:粗砂纸打磨的片刻内现象不明显。 | ||
Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出。 | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体。 | 现象三与现象一对比,说明 |
现象四:特细砂纸打磨的表面一段时间内没有明显现象。 | 现象四与现象三对比,说明 |
★影响因素:
A.打磨时用力程度及均匀程度不同
B.选用砂纸颗粒粗细程度不同
C.由于摩擦生热又形成了新的氧化膜
(4)比较步骤三各实验操作中用砂纸打磨的作用是: ▲ 。
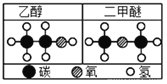
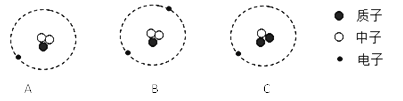
(5)请仔细观察下图:
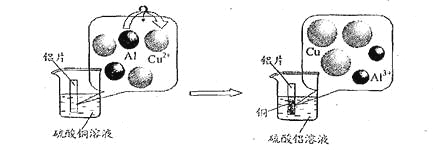
试从微观粒子变化的角度分析该反应的实质是:
▲ 。
【题目】碳酸氢钠片是一种常用药,能用于治疗胃酸过多,这是因为人体的胃液中含有盐酸。已知:NaHCO3+HCl=NaCl+H2O+CO2↑,为测定药片中碳酸氢钠的含量,小科进行了如下实验:
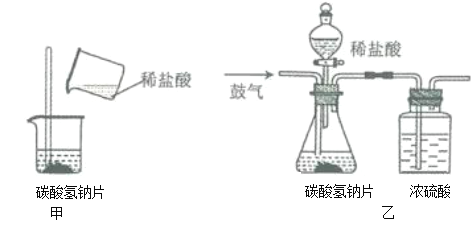
(1)小科认为,要测定药片中碳酸氢钠的含量,实验中需要采集两个数据:一是测出碳酸氢钠片样品的质量;二是根据碳酸氢钠与盐酸的反应原理,通过实验测出反应生成的_______质量。(2)小科按如图甲的实验方案,取药片和足量的稀盐酸进行实验,通过测量反应前后总质量的变化来采集实验数据。同学们认为,测得碳酸氢钠的质量分数会偏大,原因是___________________(答出一点即可)。
(3)为减小实验误差,小科又设计了如图乙的实验方案,取药片和足量的稀盐酸进行了三次实验,采集的实验数据如表:
实验序号 | 1 | 2 | 3 |
碳酸氢钠片样品质量/克 | 3.0 | 3.0 | 3.0 |
反应前总质量/克 | 193.8 | 194.6 | 193.6 |
反应后总质量/克 | 192.6 | 193.6 | 192.5 |
二氧化碳质量/克 |
请计算药片中碳酸氢钠的质量分数_____________。