题目内容
【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。
(学生实验)化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气泡逸出,写出该反应的化学方程式:_______。同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验。
(实验用品)pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
(猜想与假设)反应后溶液中溶质的组成成分可能有哪些?
猜想一:硫酸钠;猜想二:硫酸钠、碳酸氢钠;猜想三:硫酸钠、硫酸。
(实验探究)同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成下表。
实验 方案 | A | B | C | D |
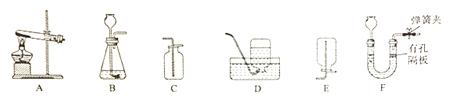
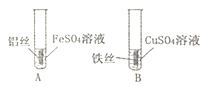
实验 操作 |
|
|
| |
实验 现象 | ________ | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH______7 | |
实验 结论 | 猜想二 不正确 | 猜想三 正确 | 猜想三正确 | 猜想三 正确 |
(得出结论)猜想三正确。
(评价反思)(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予肯定,同时指出探究中存在一处明显错误操作是______________。
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由:_______________。
(总结提高)依据所给实验用品,请你设计方案D(实验操作、实验现象)确认猜想三是正确的:_______________。
【答案】H2SO4 +2NaHCO3 = Na2SO4 + 2H2O+CO2↑ 无明显现象(变化) < 将pH试纸直接深入到溶液中会污染试剂 硫酸钠也会与氯化钡反应产生白色沉淀 取少量反应后的溶液于试管中,再加入锌片观察到有气泡产生或取少量反应后的溶液于试管中,再加入氧化铜粉末,氧化铜粉末消失,溶液有无色变为蓝色
【解析】
(1) 碳酸氢钠和稀硫酸混合,发生反应,生成硫酸钠、水和二氧化碳,故填写:
H2SO4 +2NaHCO3 = Na2SO4 + 2H2O+CO2↑;
(2猜想二中有碳酸氢钠,当滴加稀硫酸时,会产生气泡,若无明显现象,猜想二不正确,故填写:无明显现象(变化);
(3)猜想三有硫酸,当pH<7时,证明溶液中有酸,猜想三正确,故填写:<;
(4)实验方案C的操作错误,不应将pH实质伸入原溶液中会污染原溶液,故填写:将pH试纸直接深入到溶液中会污染试剂;
(5)实验方案B错误,因为硫酸钠也会与氯化钡反应产生白色沉淀,故填写:硫酸钠也会与氯化钡反应产生白色沉淀;
(6) 取少量反应后的溶液于试管中,再加入锌片观察到有气泡产生或取少量反应后的溶液于试管中,再加入氧化铜粉末,氧化铜粉末消失,溶液有无色变为蓝色

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
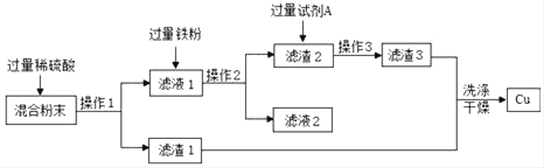
单元全能练考卷系列答案【题目】某工厂的废水中含有MgSO4和FeCl3等,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示。
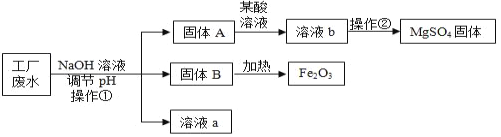
资料:部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Mg(OH)2 |
开始沉淀 | 1.9 | 9.1 |
完全沉淀 | 3.2 | 11.1 |
(1)操作①的名称__________,该工厂废水一定呈__________性。
(2)用NaOH溶液调节溶液的pH,pH的控制在__________范围内,可使废液中的铁离子(Fe3+)完全沉淀,而镁离子(Mg2+)又不损耗。
(3)操作②时,当__________即可停止加热。
(4)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为_____。
(5)溶液a除了可能含有NaOH外,还一定含有的溶质是________(填化学式)。
(6)配制2000kg质量分数为5%的氢氧化钠溶液,需要氢氧化钠______Kg。
【题目】“国庆”假期,小周对“活泼金属与硫酸溶液反应快慢的影响因素”进行了探究。
(提出问题)活泼金属与硫酸溶液反应的快慢受哪些因素的影响呢?
(猜想与假设)a.可能与硫酸溶液的质量分数有关;
b.可能与金属的形状有关;
c.可能与金属的种类有关。
(设计并实验)小周用不同质量分数的硫酸溶液和不同形状的锌进行如下实验:
实验编号 | 硫酸溶液的质量分数(均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
① | 5% | 锌粒 | 15.6 |
② | 5% | 锌片 | 25.9 |
③ | 10% | 锌粒 | 32.7 |
④ | 10% | 锌片 | 40.9 |
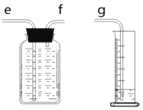
(1)小周用如图装置收集并测量氢气的体积,氢气应从_____管通入。(填e或f或g)
(2)(收集证据)要比较不同质量分数的硫酸溶液与锌反应快慢的影响,可以选择的实验编号是_____。
(得出结论)……
(反思与评价)你认为本实验设计存在哪些不足之处_____。