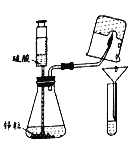题目内容
【题目】菠菜中含有草酸,将草酸晶体隔绝空气加热,使其完全分解,生成水和碳的氧化物。为了探究上述反应生成的碳的氧化物成分,同学们提出以下猜想。
(1)猜想与假设:
猜想一:只有CO;猜想二:只有CO2;猜想三:___________________。
(2)某同学设计了如下图所示实验验证猜想
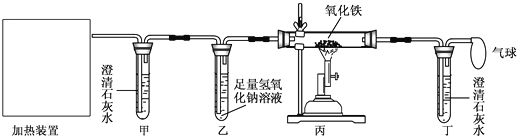
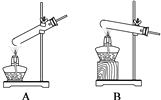
①无水草酸晶体熔点较低,加热到182℃便开始熔化,189.5℃分解。根据此信息,你应选择的加热装置为上图中______(填“A”或“B”)。
②该装置中乙的作用为______________________;末端气球的作用为____________________。
③实验中下列操作的先后顺序是______________________。
a.点燃加热装置中的酒精灯 b.点燃丙处的酒精喷灯 c.检查装置气密性 d.装入药品
④若甲试管和丁试管内溶液都变浑浊,丙处玻璃管内的黑色固体变成红色,则猜想__________正确。
【答案】 既有CO,又CO2 A 吸收二氧化碳 吸收尾气防止空气污染 cdab 三
【解析】菠菜中含有草酸,将草酸晶体隔绝空气加热,使其完全分解,生成水和碳的氧化物。(1)猜想与假设:猜想一:只有CO;猜想二:只有CO2;猜想三:既有CO,又CO2 。(2)①无水草酸晶体熔点较低,加热到182℃便开始熔化,189.5℃分解。根据此信息,应选择的加热装置为右图中A。②该装置中乙的作用为吸收二氧化碳;末端气球的作用为. 吸收尾气防止空气污染。③实验中下列操作的先后顺序是 c.检查装置气密性 d.装入药品a.点燃加热装置中的酒精灯 b.点燃丙处的酒精喷灯。④若甲试管和丁试管内溶液都变浑浊,丙处玻璃管内的黑色固体变成红色,则猜想三正确。
点睛∶本题主要考查探究草酸晶体隔绝空气加热,完全分解,生成水和碳的氧化物成分。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
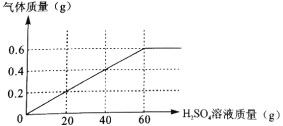
小学生10分钟应用题系列答案【题目】兴趣小组想测定某铁合金中铁的含量,做了如下实验,称取14克样品,放入质量为50克的烧杯中,再往烧杯中加入100克足量的稀硫酸(杂质碳不与酸反应,也不溶于水),
并对烧杯进行了四次称量,记录数据如下:
反应时间 | T0 | T1 | T2 | T3 |
烧杯总质量(克) | 164 | 163.8 | 163.6 | 163.6 |
求(1)反应产生的氢气的质量是多少?
(2)该样品中铁的质量分数是多少?
(3)反应后所得溶液中溶质质量分数是多少?(要求写出计算过程,结果精确到0.1%)