题目内容
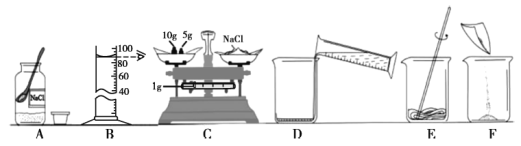
【题目】氯气是一种重要的工业原料。下图是实验室制取收集氯气以及验证氯气性质的实验装置图。
[查阅资料]氯气是一种黄绿色的剧毒气体,密度大于空气。
制取氯气的化学方程式:2KMnO4+16HCl═2MnCl2+2KCl+5Cl2↑+8H2O。
氯气与水反应的化学方程式:Cl2+H2O═HCl+HClO。
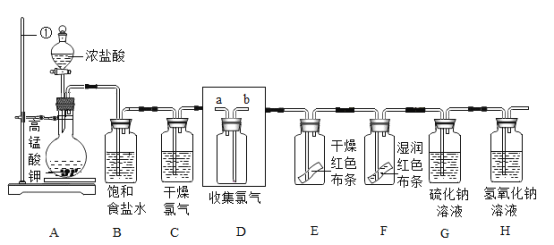
(1)A中仪器①的名称是__,实验时连接好仪器,要先__(填操作名称)再装药品。
(2)从A装置中出来的Cl2混有H2O和__(填化学式),C装置中的试剂是__,C装置的导管应该与D装置导管口__(填“a”或“b”)端连接。
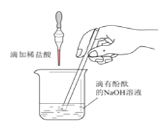
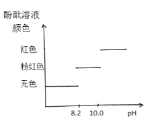
(3)E中红色布条不褪色,F中红色布条褪色,说明Cl2没有漂白性,而是Cl2与水反应生成的___(填化学式)有漂白性。
(4)G中出现淡黄色沉淀,说明反应生成了硫单质,该反应的化学方程式为____。
(5)H是尾气(Cl2)处理装置,反应的化学方程式为____。
【答案】铁架台 检查气密性 HCl 浓硫酸 b HClO Cl2+Na2S═S↓+2NaCl Cl2+2NaOH═NaCl+NaClO+H2O 。
【解析】
(1)①为固定装置的铁架台;有气体参与的实验,实验开始前需要检查装置的气密性;(2)由于浓盐酸具有挥发性,所以制备的氯气中混有挥发出的氯化氢;浓硫酸具有吸水性,干燥气体时常用的液体干燥剂为浓硫酸;由于氯气密度比空气大,现在瓶内底部聚集,所以从长口b进气,短口a排气,达到手收集气体的目的;
(3)氯气与水反应生成盐酸和次氯酸,由于次氯酸根(HClO)具有强氧化性,所以具有漂白性;
(4)反应物氯气和硫化钠,生成物有硫单质和氯化钠的化学方程式:Cl2+Na2S═S↓+2NaCl。
(5)氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水的化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O。

 名校课堂系列答案
名校课堂系列答案