题目内容
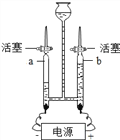
【题目】同学们应用数字化实验探究外界条件对双氧水分解速率的影响。实验装置如图:
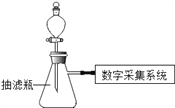
【进行实验】
序号 | 主要实验步骤 | 装置内压强时间图象 |
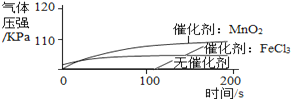
实 验 1 | ①1号抽滤瓶中不加任何试剂, 2号抽滤瓶中加入0.2 g MnO2粉末, 3号抽滤瓶中加入0.2 g FeCl3粉末。 ②用三支分液漏斗分别加入15 mL 4%的H2O2溶液。 |
|
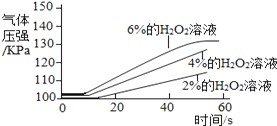
实 验 2 | ①三个抽滤瓶中分别加入0.2 gFeCl3粉末。 ②分别用1号分液漏斗加入15 mL2%的H2O2溶液;用2号分液漏斗加入15 mL4%的H2O2溶液;用3号分液漏斗加入15 mL6%的H2O2溶液。 |
|
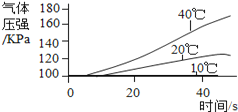
实 验 3 | ①三个抽滤瓶中分别加入0.2 gFeCl3粉末,分别放入装有10℃、20℃、40℃水的水槽中。 ②用三支分液漏斗分别加入15 mL4%的H2O2溶液。 |
|
【解释与结论】
(1)某同学得到“不同催化剂的催化效果不同”的结论,他的依据是_________________________。
(2) 通过上述实验得到:影响该反应速率的外界因素有___________________________________。
【反思与评价】(3)经过多次实验,有的同学对比实验1的3号瓶、实验2的2号瓶中同为40s时的气体压强,发现存在较大的差异,可能的原因是___________________________________________。
【答案】 实验1中2,3号瓶曲线不同 催化剂种类,反应物浓度,温度 实验温度不同
【解析】 (1)得到“不同催化剂的催化效果不同”的结论,他的依据是实验1中2,3号瓶内催化剂不同,曲线不同;(2) 实验1可得,催化剂的种类影响反应速率,由实验2可得,反应物的浓度影响反应速率;实验3可得温度影响反应速率; (3)经过多次实验,有的同学对比实验1的3号瓶、实验2的2号瓶中同为40s时的气体压强,发现存在较大的差异,可能的原因是实验温度不同,温度越高,反应越快,相同时间内产生气体多,压强大,反之,压强小。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】同学们在学习碱的化学性质时,进行了如图所示的实验: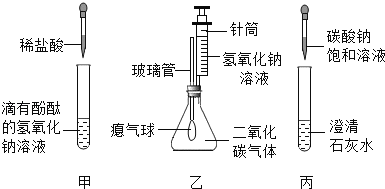
(1)乙实验中滴加氢氧化钠溶液后,可观察到的现象是 ,发生反应的化学方程式为 .
(2)丙实验中观察到的实验现象是 .
(3)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问.
【提出问题】废液中含有哪些物质?
【交流讨论】
①一定含有的物质:指示剂、水、硫酸钠、碳酸钙.
②还含有能使废液呈碱性的物质,能使废液呈碱性的物质是什么?
同学们有如下猜想:
小丽认为:有氢氧化钠和碳酸钠
小明认为:只有碳酸钠
小平认为:只有氢氧化钠
你认为可能的是 (写一种猜想).
【实验设计】小芳想用氯化钙溶液来验证以上三个同学的猜想,通过查阅资料获悉氯化钙溶液呈中性,并设计如下实验,请你将小芳的实验设计补充完整.
实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置 | ①有白色溶液,溶液呈红色 | 小丽的猜想正确 |
② | 小明的猜想正确 | |
③ | 小平的猜想正确 |