题目内容
【题目】水是生命的源泉,也是不可缺少的资源.
①自然界的水常常遭到污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,人们把这种现象称之为水质富营养化.这里的“氮和磷”是指_____;(填字母)
A元素 B原子 C离子 D分子
②净水器常用活性炭,主要是利用活性炭的_____性.生活中,既能降低水的硬度,又能杀菌消毒的方法是_____.
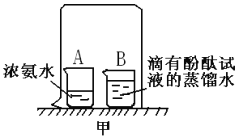
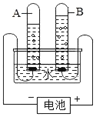
③电解水的装置如图所示,管A,管B中的气体质量比是_____.
④为了防止水的污染,下列做法有利于保护水资源的是_____(填编号).
A抑制水中所有动、植物的生长;
B不任意排放工业废水;
C大量使用化肥农药;
D生活污水经过净化处理后再排放.
⑤在化学实验和科学研究中,水也是一种常用的试剂.水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+).下列对上述过程的描述不合理的是_____(填序号).
A氧元素发生了改变 B粒子的组成发生了改变
C粒子的化学性质发生了改变 D水分子与水合氢离子的电子数不同.
【答案】A 吸附 煮沸 1:8 BD AD
【解析】
①物质的组成常用元素来描述,自然界的水常常遭到人为污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,这里的“氮和磷”是指元素,故选A。
②净水器常用活性炭,主要是利用活性炭的吸附性,生活中,既能降低水的硬度,又能杀菌消毒的方法是煮沸。
③由电解水的装置可知,管A收集到的气体较多是氢气,则管B中收集到的气体是氧气,二者的质量比是1:8。
④A、抑制水中所有动植物的生长,不能保持生态平衡,不能防止水污染,故A不正确;
B、不任意排放污水有利于保护水资源,故B正确;
C、大量使用农药和化肥,会严重污染水源,同时也会造成粮食污染,故C不正确;
D、生活污水经过净化处理后再排放,有利于保护水资源,故D正确。故选BD。
⑤H+和水结合形成水合氢离子的方程式为H++H2O=H3O+,根据质量守恒定律可知,元素种类没有变化,微粒组成由分子和离子结合成为离子而发生变化,化学性质也变为酸性,氢离子中没有电子,水合过程前后电子总数均为10电子,无变化,故选AD。

【题目】某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如表实验数据:
实验次数 | 一 | 二 | 三 | 四 |
固体混合物的质量(g) | 20 | 20 | 20 | 20 |
加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
问:(1)表中m的值为_____;
(2)哪次实验恰好完全反应_____;求该次反应后所得溶液中氯化钠的质量共多少克_____?