题目内容
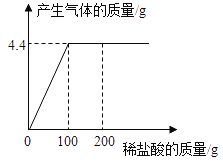
【题目】向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法正确到是( )
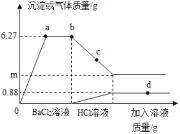
A. 0﹣a段发生了一个反应
B. c点沉淀的成分为一种
C. 取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量
D. m=2.33
【答案】D
【解析】
A、0﹣a段发生了2个反应,即氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,和硫酸钠反应生成硫酸钡沉淀和氯化钠,该选项说法不正确;
B、c点沉淀的成分为2种,即硫酸钡和没有反应的碳酸钡,该选项说法不正确;
C、取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,不能说明加入的盐酸已过量,这是因为稀盐酸和碳酸钡反应生成的氯化钡能和硝酸银反应生成白色沉淀氯化银,该选项说法不正确;
D、设碳酸钡质量为x,
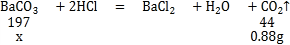
![]()
x=3.94g,
则m=6.27﹣3.94=2.33,故该选项说法正确。

 53随堂测系列答案
53随堂测系列答案【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。
Ⅰ.定性探究
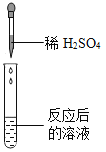
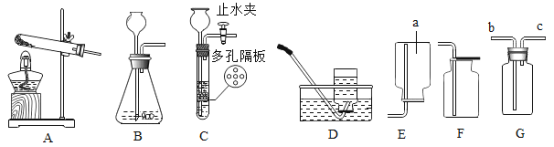
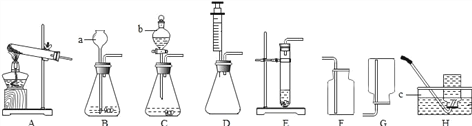
化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气体逸出,写出该反应的化学方程式_________________________,同学们对反应后溶液中溶质的成分进行了探究。认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验:
(实验用品)pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
(猜想与假设)反应后溶液中溶质的可能组成成分
猜想一:硫酸钠 猜想二:硫酸钠、碳酸氢钠 猜想三:硫酸钠、硫酸
(实验探究)同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成下表实验现象中的①②③。
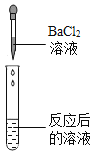
实验方案 | A | B | C | D | |
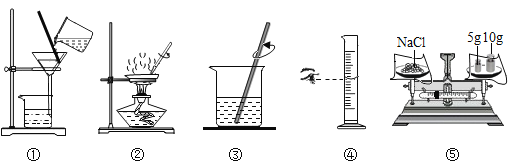
实验操作 |
|
|
|
| |
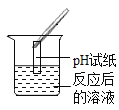
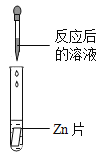
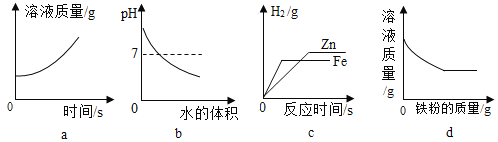
实验现象 | ________ | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH________7 | _________ | |
实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
(得出结论)猜想三正确。
(评价反思)
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显操作错误是:_____;
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由________。
(总结提高)依据所给实验用品,设计不同的方案确认猜想三是正确的。请写出你的实验方案________。
Ⅱ.定量探究
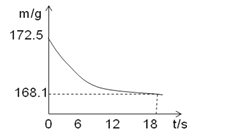
(1)取一定量的碳酸氢钠样品,加入到盛有足量稀硫酸的烧杯中(烧杯质量为118.1克),不断用玻璃棒搅拌。反应过程用精密仪器测得烧杯和混合物的总质量(m)与反应时间(t)关系如图所示,求所得溶液中溶质质量分数________。