题目内容
【题目】碳酸二甲酯被称为绿色化学试剂,可以代替光气、硫酸二甲酯等剧毒原料,同时它还是良好剂和燃油添加剂。碳酸二甲酯的化学式为C3H6O3,试计算:
(1)碳酸二甲酯的化学式量为________.
(2)碳酸二甲酯中碳、氢、氧三种元素的质量比为(化成最简整数比)_____________
(3)碳酸二甲酯中碳元素的质量分数为:C%=_________(写出计算过程)
(4)180g碳酸二甲酯中碳元素的质量为______g
【答案】90 6:1:8 ![]() 72
72
【解析】
(1)碳酸二甲酯的化学式量为:12×3+1×6+16×3=90,故填:90;
(2)碳酸二甲酯中碳、氢、氧三种元素的质量比为:(12×3):(1×6):(16×3)=6:1:8;
(3)碳酸二甲酯中碳元素的质量分数为:C%=![]() =
=![]() =40%
=40%
(4)180g碳酸二甲酯中碳元素的质量为:180g×40%=72g。

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
【题目】化学概念在逻辑上存在如图所示关系,对下列概念的说法不正确的是( )
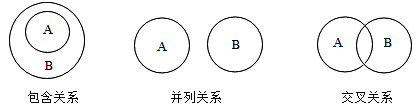
A.单质与化合物属于交叉关系B.化合物与氧化物属于包含关系
C.氧化反应与化合反应属于交叉关系D.分解反应与化合反应属于并列关系
【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是 ( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
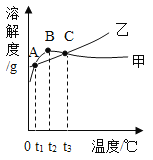
A.甲为NH4Cl
B.t2℃应介于30℃~50℃
C.甲、乙饱和溶液从t3℃降温到t2℃,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1℃升温到t3℃,为使其溶液恰好饱和,加入的甲、乙固体质量相等