题目内容
【题目】实验是科学探究的重要途径。
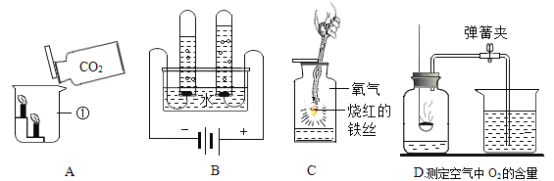
(1)某同学利用如图微型装置进行实验探究。请回答:
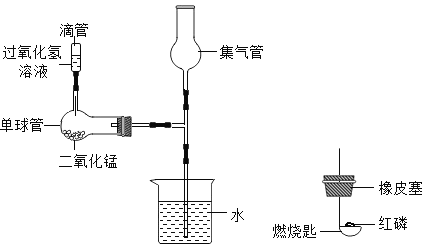
①单球管中反应的化学方程式是_____________________________________。
②制取的气体收集在集气管中,将红磷在酒精灯上加热后迅速放进集气管,塞紧塞子,观察到的现象是______________________。反应的化学方程式为________________。
(2)实验室选用以下装置制取纯净、干燥的![]() ,并验证其部分性质。
,并验证其部分性质。
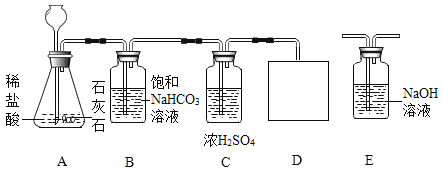
①B装置的作用是________________________________。
②请在D中简要补画出![]() 的收集装置图_____________
的收集装置图_____________
③要证明在E装置中![]() 与NaOH溶液发生了反应,请你设计实验证明,写出实验步骤、现象和结论。_____________
与NaOH溶液发生了反应,请你设计实验证明,写出实验步骤、现象和结论。_____________
(3)取12.5 g石灰石于装置A中,向其中加入100 g足量的稀盐酸,充分反应后(杂质不参加反应),A中固液混合物的质量为108.1 g,请计算该石灰石中碳酸钙的质量分数。_____________
【答案】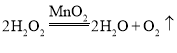 产生大量白烟,放出大量热
产生大量白烟,放出大量热 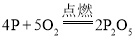 除去
除去![]() 去杂质HC1
去杂质HC1 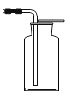 取适量的反应后溶液加入适量的氯化钙溶液,若产生白色沉淀,则CO2与NaOH溶液发生了反应 80%
取适量的反应后溶液加入适量的氯化钙溶液,若产生白色沉淀,则CO2与NaOH溶液发生了反应 80%
【解析】
(1)在单球管中,过氧化氢在二氧化锰催化作用下分解生成水和氧气,发生反应的化学方程式是: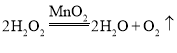 ;
;
制取的气体收集在集气管中,将红磷在酒精灯上加热后迅速放进集气管,塞紧塞子,观察到的现象是红磷燃烧,产生大量白烟,放出大量热,磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为: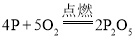 ;
;
(2)①B装置中,碳酸氢钠和稀盐酸中挥发出的氯化氢反应生成氯化钠、水和二氧化碳。B装置的作用是除去![]() 去杂质HC1;
去杂质HC1;
②二氧化碳密度比空气大,可以用向上排空气法收集,如下图所示: ;
;
③④要证明在E装置中CO2与NaOH溶液发生了反应,可选用的试剂是氯化钙溶液,这是因为氯化钙能和氢氧化钠与二氧化碳反应生成的碳酸钠反应生成碳酸钙沉淀和氯化钠。实验步骤、现象和结论是取适量的反应后溶液加入适量的氯化钙溶液,若产生白色沉淀,则CO2与NaOH溶液发生了反应;
(3)反应放出![]() 质量为
质量为![]() ;
;
设:参加反应![]() 质量为x。
质量为x。
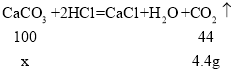
![]()
石灰石中碳酸钙的质量分数=![]() 。
。
答:石灰石中![]() 质量分数为80%。
质量分数为80%。

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案【题目】网络上有一段视频:将“锡纸”剪成一段两头宽中间窄的纸条,然后两头分别连接电池的正负极,观察到“锡纸”立即燃烧。据此,小力同学取某种“锡纸”进行了以下探究:
(1)探究“锡纸”燃烧的原因:“锡纸”两端连接电池两极后造成短路致使“锡纸”燃烧,从燃烧的条件开始“锡纸”不燃烧但短路后却能燃烧的原因是_____________
(2)探究“锡纸”中金属的成分:
(查阅资料)①“锡纸”是锡箔或铝箔;②锌粉是一种深灰色固体;③锡(Sn)与酸或盐溶液反应生成正二价的锡盐。
(提出猜想)猜想I:“锡纸”中的金属是锡;
猜想I I:“锡纸”中的金属是铝。
(进行实验)设计方案并进行实验
实验操作 | 实验现象 | 实验分析与结论 |
取打磨后的“锡纸”片放入试管中,滴加氯化锌溶液 | “锡纸”表面有深灰色固体析出 |
根据实验现象,结合金属活动性顺序可知猜想______________(填“I”或"II")成立;反应的化学方程式为______________________
(交流讨论)①实验中打磨“锡纸”的目的是_____________
②下列物质的溶液可以替代氯化锌溶液完成上述实验的是______________(序号)
A 硫酸铜 B 硝酸银 C 氯化钠 D 硫酸亚铁
(拓展应用)电器短路会引起火灾,我们要严加防范。如果电器着火应该采取的灭火方法是____.