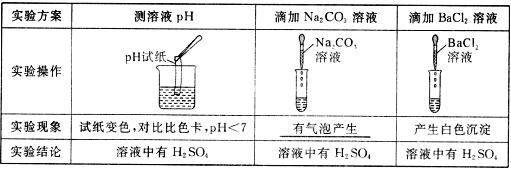
题目内容
【题目】草木灰是一种农家肥料,其主要成分是碳酸钾(K2CO3 ),某兴趣小组同学对草木灰的成分产生兴趣,进行了如下实验探究。
(提出问题)草木灰中含有碳酸钾吗?
(查阅资料)①碳酸钾呈无色晶体状或白色颗粒状固体,易溶于水,水溶液呈碱性。
②钾离子的检验方法:将铂丝蘸稀盐酸在酒精灯火焰上灼烧至无色,蘸取试样在酒精灯火焰上灼烧,透过蓝色钴玻璃观察火焰颜色,若火焰呈紫色则含有钾离子。
(进行实验)
取少量草木灰放入一只洁净烧杯中,加入足量水充分搅拌,静置,待用。
任务一:将铂丝蘸稀盐酸在酒精灯火焰上灼烧至无色,蘸取烧杯中上层清液少许在酒精灯火焰上灼烧,透过蓝色钴玻璃观察火焰颜色,火焰呈紫色,则溶液中含有__________(填离子符号)。
任务二:下面为同学们设计的检验 CO32- 实验方案:
方案 1:甲同学设计了如下实验方案
实验步骤 | 实验现象 | 实验结论 |
取上述烧杯中少量上层清液于试管中,滴加足量稀盐酸 | ___________ | 溶液中含有 CO32- |
乙同学对甲同学的方案提出质疑:认为要证明 CO32- 存在,还需进一步证明_________________,检验的化学反应方程式为_______________。
方案 2:丙同学设计了如下方案。用pH试纸测定上层溶液的酸碱性,pH>7,溶液中含有CO32-,具体操作方法是____________。
丁同学对上述方案产生质疑:认为溶液 pH>7,草木灰中可能含有氢氧化钾。同学们针对丁同学的质疑又进行了如下实验:取少量上层溶液于试管中,滴加足量 CaCl2 溶液,充分反应后过滤,向滤液中滴几滴_______________溶液。滴加足量 CaCl2 溶液的作用是_______________。
(反思提高)草木灰作为肥料,适宜在____________(填“酸”“碱”或“中”)性土壤中施用。
【答案】K+ 有气泡产生 生成气体是否为二氧化碳 ![]() 用玻璃棒蘸取少量液体,滴在pH试纸上,将试纸显示的颜色与标准比色卡比对 CuSO4(或 FeCl3 或无色酚酞)(合理即可) 除去溶液中的碳酸根离子 酸
用玻璃棒蘸取少量液体,滴在pH试纸上,将试纸显示的颜色与标准比色卡比对 CuSO4(或 FeCl3 或无色酚酞)(合理即可) 除去溶液中的碳酸根离子 酸
【解析】
{进行实验}任务一:由查阅资料可知,含有钾离子的溶液灼烧时,透过蓝色钴玻璃观察到火焰颜色呈紫色,所以该溶液中含有钾离子,钾离子的化学式为K+,故填K+;
任务二:方案1:如果溶液中含有碳酸根离子,加入稀盐酸后,会生成二氧化碳气体,产生的现象是产生气泡,故填有气泡产生;
能与稀盐酸反应生成气体,不一定是二氧化碳,还需要检验生成的气体是否是二氧化碳,故填生成气体是否为二氧化碳;
化学上检验二氧化碳的方法是将气体通入澄清的石灰水中,因为二氧化碳能与石灰水中的氢氧化钙反应生成水和碳酸钙沉淀使石灰水变浑浊,故反应的化学方程式写为:Ca(OH)2+CO2=CaCO3↓+H2O。
方案2:化学上用pH试纸测溶液pH的方法是用玻璃棒蘸取少量液体,滴在pH试纸上,将试纸显示的颜色与标准比色卡比对,故填用玻璃棒蘸取少量液体,滴在pH试纸上,将试纸显示的颜色与标准比色卡比对;
氢氧化钾溶液呈碱性,能够使无色的酚酞溶液变红,且氢氧化钾还能与硫酸铜生成蓝色沉淀氢氧化铜,能与氯化铁反应生成红褐色沉淀氢氧化铁,所以检验氢氧化钾的存在时,可先向溶液中滴加足量 CaCl2 溶液,充分反应后过滤,向滤液中滴几滴硫酸铜溶液,或酚酞溶液,或氯化铁溶液来检验氢氧化钾是否存在,故填CuSO4(或 FeCl3 或无色酚酞);
滴加足量的CaCl2 溶液能与溶液中的碳酸根完全反应生成沉淀,避免碳酸钾对检验氢氧化钾的存在产生干扰,故填除去溶液中的碳酸根离子。
{反思提高}碳酸钾的水溶液呈碱性,能与酸发生中和反应,所以草木灰适宜在酸性土壤中施用,故填酸。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案