题目内容
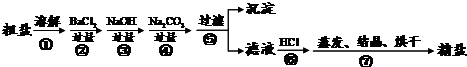
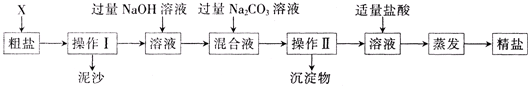
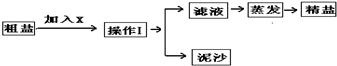
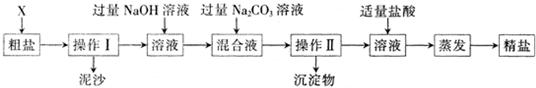
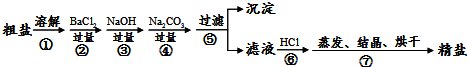
26、通过海水晾晒可得粗盐,粗盐除NaCl外,还含有CaCl2、Na2SO4以及泥沙等杂质.由粗盐制备精盐的操作流程如下:
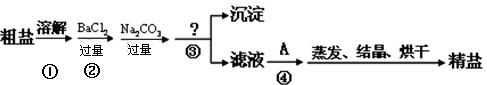
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,其作用是
(2)第②步加试剂的目的是除去粗盐中的

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,其作用是
加速粗盐溶解
.第③步的操作名称是过滤
.(2)第②步加试剂的目的是除去粗盐中的
Na2SO4
(填化学式),第④步中加入的试剂A是HCl
(填化学式).分析:(1)根据玻璃棒在溶解时所起的作用解答,
根据粗盐提纯的步骤顺序分析解答.
(2)分析钡离子可以将哪种离子转化成沉淀,
分析通过①②③步以后,溶液中所剩的离子有哪些,再选择试剂.
根据粗盐提纯的步骤顺序分析解答.
(2)分析钡离子可以将哪种离子转化成沉淀,
分析通过①②③步以后,溶液中所剩的离子有哪些,再选择试剂.
解答:解:(1)在①步中用玻璃棒搅拌,实际上加速了溶液的流动性,溶液流动快了,对固体的洗涮就快了,也就加速了固体的溶解,故答案为:加快粗盐溶解,
粗盐提纯的一般步骤是:溶解、过滤、蒸发、结晶,③步后出现了沉淀和液体两部分,故答案为:过滤;
(2)除杂质的实质是除去杂质离子,而加入的氯化钡中的氯离子对氯化钠来说不算杂质,与钡离子生成沉淀的只能是硫酸钠,将硫酸钠转化成硫酸钡沉淀和氯化钠,
故答案为:Na2SO4;
在经过①②③步后,溶液中的杂质离子只剩下碳酸根离子了,要除去碳酸根离子又不能引入新的杂质,只能加盐酸除去,故答案为:HCl.
粗盐提纯的一般步骤是:溶解、过滤、蒸发、结晶,③步后出现了沉淀和液体两部分,故答案为:过滤;
(2)除杂质的实质是除去杂质离子,而加入的氯化钡中的氯离子对氯化钠来说不算杂质,与钡离子生成沉淀的只能是硫酸钠,将硫酸钠转化成硫酸钡沉淀和氯化钠,
故答案为:Na2SO4;
在经过①②③步后,溶液中的杂质离子只剩下碳酸根离子了,要除去碳酸根离子又不能引入新的杂质,只能加盐酸除去,故答案为:HCl.
点评:本题主要考查了粗盐提纯的一般步骤,以及除杂质的原则是不能引入新的杂质.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
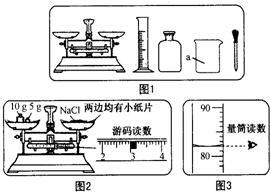 某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验:
某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验: