题目内容
【题目】分析处理图表中的信息是学习化学的一种重要方法。
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
①30℃时,KNO3溶液的最大浓度(溶质质量分数)为______(只列计算式,不需要计算结果)。
②根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X.则X的取值范围是______。
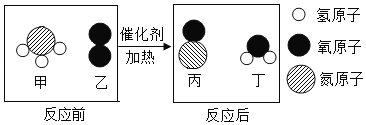
(2)根据图电解水的实验,回答下列问题:
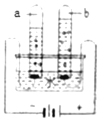
①从宏观上观察:图示a、b管中产生的体积比约为2:1,则他们的质量比为______。
②从微观上下列说法错误的是______(填字母)。
A.水是由水分子构成的
B.水是由氢原子和氧原子构成的
C.每个水分子是由2个氢原子和1个氧原子构成的
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答:
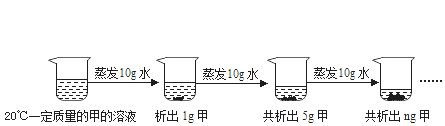
①蒸发前原溶液是______(填“饱和”或“不饱和”)固体n的数值是______。
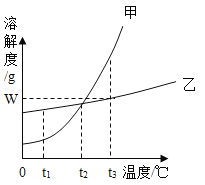
②依据上述实验,你认为甲的溶解度随温度变化的趋势是______(填字母)。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
【答案】45.8/(100g+45.8g)×100% 36~36.3 1:8 B 不饱和 9 C
【解析】
(1)①30℃时,硝酸钾的溶解度是45.8g,所以KNO3溶液的最大浓度(溶质质量分数)为:45.8/(100g+45.8g)×100%;
②根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,所以X的取值范围是36~36.3;
(2)①水在通电的条件下生成氢气和氧气,正氧负氢,体积比是1:2,质量比是8:1,所以图示a、b管中产生的体积比约为2:1,他们的质量比为1:8;
②A、水是由水分子构成的,故正确;
B、水分子是由氢原子和氧原子构成的,故错误;
C、每个水分子是由2个氢原子和1个氧原子构成的,故正确;
故选:B;
(3)①第一次蒸发析出1g晶体,第二次蒸发共析出5g晶体,说明饱和状态时蒸发10g水最多析出4g晶体,所以蒸发前原溶液是不饱和,固体n的数值是9;
②蒸发溶剂的方法,溶液中都会析出晶体,所以依据上述实验,甲的溶解度随温度变化的趋势是无法判断,故选:C。

【题目】某化学兴趣小组的同学要探究铝、铁、铜三种金属的活动性顺序,请你参与探究并填写空格。
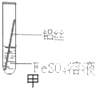
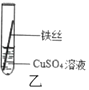
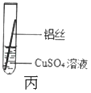
(实验探究)同学们将粗细相同的、打磨过的铝丝和铁丝分别插入硫酸亚铁溶液、硫酸铜溶液中:
操 作 |
|
|
| 根据现象得出金属活动的顺序 |
现象 | 铝丝表面附着银白色固体 | _____ | 铝丝表面附着红色固体 | _____ |
写出铝与硫酸铜溶液反应的化学方程式_____。
(交流讨论)
(1)同学们经讨论后认为上述方案可以优化,_____(选填“甲“、“乙“或“丙”)试管的实验时是多余的。
(2)洁洁认为,只用一支盛有少量稀硫酸的试管,合理安排金属丝的插入顺序(能与稀硫酸反应的要一次将稀硫酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序,他设计了两种插入顺序,请你补全顺序二:
顺序一:Cu Fe Al:顺序二:_____。
洁洁按顺序一做实验时,发现铁丝放入稀硫酸中片刻后无气泡产生,几分钟后才有少量气泡产生,你认为可能的原因是_____。