题目内容
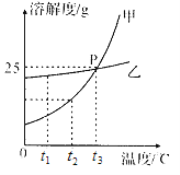
【题目】下图是甲、乙两种固体物质的溶解度曲线,请根据图示回答:
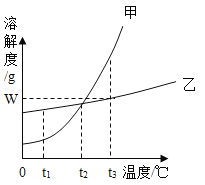
(1)t1℃时,甲的溶解度________乙的溶解度(填“>”、“<”或“=”);
(2)要使接近饱和的甲溶液变成饱和溶液,可采取的方法是_____________;
(3)甲、乙各wg分别加入到两只盛有100g水的烧杯中,充分搅拌,在t3℃时所得甲溶液为________溶液(填“饱和”或“不饱和”);
(4)在t2℃时,乙的饱和溶液中含少量的甲,要制得较纯的乙晶体,可采取_______方法.
【答案】< 增加溶质、蒸发溶剂,降低温度 不饱和 蒸发结晶
【解析】
(1)根据图示可知:t1℃时,甲的溶解度曲线上的点在乙曲线的下方,故此温度时甲的溶解度小于乙的溶解度;
(2)要使接近饱和的甲溶液变为饱和溶液可采取的方法是:增加溶质、蒸发溶剂,降低温度;
(3)在t3℃时,甲的溶解度大于Wg,故t3℃时,甲wg加入到盛有100g水的烧杯中,充分搅拌,所得甲溶液为不饱和溶液;
(4)由溶解度曲线可知,乙随温度的变化溶解度变化不大,故应可采取蒸发结晶方法制得乙晶体。

 阅读快车系列答案
阅读快车系列答案【题目】分析处理图表中的信息是学习化学的一种重要方法。
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
①30℃时,KNO3溶液的最大浓度(溶质质量分数)为______(只列计算式,不需要计算结果)。
②根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X.则X的取值范围是______。
(2)根据图电解水的实验,回答下列问题:
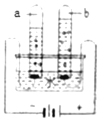
①从宏观上观察:图示a、b管中产生的体积比约为2:1,则他们的质量比为______。
②从微观上下列说法错误的是______(填字母)。
A.水是由水分子构成的
B.水是由氢原子和氧原子构成的
C.每个水分子是由2个氢原子和1个氧原子构成的
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答:
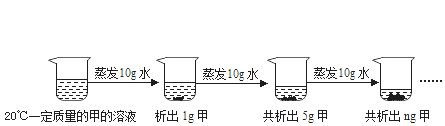
①蒸发前原溶液是______(填“饱和”或“不饱和”)固体n的数值是______。
②依据上述实验,你认为甲的溶解度随温度变化的趋势是______(填字母)。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断