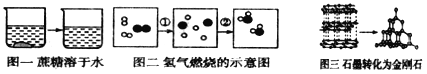
题目内容
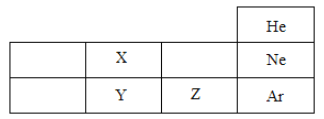
【题目】一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示:

下列说法正确的是( )
A. x的值为36 B. 该反应属于化合反应
C. W由碳、氢两种元素组成 D. W中碳、氢元素质量比为1:3
【答案】C
【解析】
A、x=100-52-3=45,该选项说法不正确;
B、反应后W质量是0,是反应物,氧气质量分数减小,是反应物,二氧化碳和水的质量分数增大,都是生成物,该反应不是化合反应,该选项说法不正确;
C、反应后二氧化碳和水的质量分数都增大,说明W和氧气反应生成二氧化碳和水,生成的二氧化碳和水中的碳元素、氢元素来自于W,因此W中含有碳元素、氢元素,W中氧元素质量分数为:(52%-8%)×32/44+(45%-9%)×16/18-(67%-3%)=0,即W中不含有氧元素,该选项说法正确;
D、W中碳、氢元素质量比为:(52%-8%)×12/44:(45%-9%)Z/18=3:1,该选项说法不正确。
故选:C

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室常用双氧水与二氧化锰混合来制取氧气,写出相关反应的化学方程式:_____,小王同学对“双氧水分解快慢的影响因素”进行了探究.
(提出问题)双氧水分解快慢的影响因素有哪些?
(猜想与假设)猜想一:可能与二氧化锰的形状有关;猜想二:可能与温度有关.
(设计并实验)小王同学用8mL3%的双氧水和二氧化锰进行了如下实验(反应进行10s时,H2O2均有剩余);
实验编号 | 温度℃ | 二氧化锰的形状(均取0.4cm) | 收集到氧气的体积/mL(时间均为10s) |
① | 20 | 颗粒状 | a |
② | 30 | 粉末状 | b |
③ | 30 | 颗粒状 | c |
④ | 20 | 粉末状 | d |
(1)欲探究温度对”双氧水分解快慢“是否有影响,应该比较_____和_____(填“a”“b”“c”或“d”)的大小;若粉末状二氧化锰催化效果好,那么_____>_____(填“a”“b”“c”或“d”)
(2)其他条件相同,双氧水浓度可能会影响催化效果,请你设计实验方案进行验证:_____.
(3)小王同学还是用了压强传感器测不同质量二氧化锰对双氧水分解快慢的影响.他在8mL3%的双氧水中分别加入了0.03g,0.06g,0.08g,0.12g,0.24gMnO2.测得容器内压强的变化曲线如图所示(曲线的斜率表征催化反应的速率).请你观察图,并写出两条规律性结论:
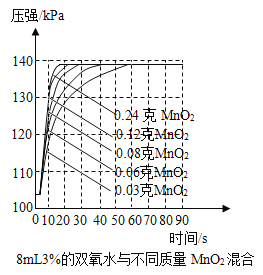
①_____;
②_____.
【题目】实验室通常利用如图装置制取氧气。

写出KClO3在MnO2作用下制取氧气的化学方程式______;
某化学兴趣小组在实验过程中发现有以下“异常”现象:
a.利用排空法收集氧气有异味;
b.颗粒状MnO2变得更细。
对此进行了以下探究:
探究(I)利用排空法收集的氧气有异味
查阅资料:KClO3在MnO2作用下分解生成氧气,经历了以下三个过程
①2KClO3+2MnO2![]() 2______+Cl2↑+O2↑
2______+Cl2↑+O2↑
②2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
③Cl2+K2MnO4![]() 2KCl+MnO2+O2↑;
2KCl+MnO2+O2↑;
(1)写出横线物质的名称______,其中Mn元素的化合价为______;
(2)猜测“利用排空法收集氧气有异味”的物质是______。
探究(Ⅱ)颗粒状MnO2变得更细
学习小组通过讨论猜测:是因为MnO2也参加了化学反应。小组同学共同设计实验并验证MnO2在该反应中作催化剂。
实验操作 | 实验现象 | 解释 | |
实验一 | 将KClO3加热至融化,伸入带火星的木条。 | 木条一段时间后复燃 | KClO3受热要分解产生氧气; |
实验二 | 加热MnO2,伸入带火星的木条 | ______ | MnO2受热不产生氧气; |
实验三 | 取适KClO3和2g的 ______ | 木条迅速复燃 | MnO2 ______ (填“加快”或“减慢”)KClO3的分解 |
实验结论:MnO2是KClO3受热分解的催化剂。
归纳反思:该小组的实验结论受到其他小组的质疑,为此该小组又补充以下实验:
(1)待试管完全冷却后,向实验三的试管中加蒸馏水,将混合物全部转移至烧杯,过滤(MnO2不溶于水,其他物质均能溶于水),洗涤沉淀,烘干,称量,目的是验证______;称量所得固体质量______;
(2)设计实验验证催化剂的另一个特点,实验方案______。
【题目】分析处理图表中的信息是学习化学的一种重要方法。
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
①30℃时,KNO3溶液的最大浓度(溶质质量分数)为______(只列计算式,不需要计算结果)。
②根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X.则X的取值范围是______。
(2)根据图电解水的实验,回答下列问题:
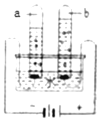
①从宏观上观察:图示a、b管中产生的体积比约为2:1,则他们的质量比为______。
②从微观上下列说法错误的是______(填字母)。
A.水是由水分子构成的
B.水是由氢原子和氧原子构成的
C.每个水分子是由2个氢原子和1个氧原子构成的
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答:

①蒸发前原溶液是______(填“饱和”或“不饱和”)固体n的数值是______。
②依据上述实验,你认为甲的溶解度随温度变化的趋势是______(填字母)。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断