题目内容
【题目】图为元素周期表中钠元素的相关信息,下列说法正确的是 ( )
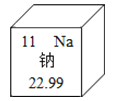
A.钠原子核内质子数为11
B.钠为非金属元素
C.钠原子的实际质量为22.99 g
D.钠元素的原子结构示意图为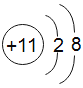
【答案】A
【解析】
A、在元素周期表中,元素名称左上方的数字表示原子序数,原子序数=原子核内质子数=11,符合题意;
B、由“钅”字旁可知,钠为金属元素,不符合题意;
C、在元素周期表中,元素名称下方的数字表示相对原子质量,钠原子的相对原子质量为22.99,原子的相对原子质量等于原子的实际质量与碳12质量的1/12的比值,相对原子质量的单位“1”不是“g”,常省略不写,不符合题意;
D、钠元素的原子核外电子数=原子序数=11,根据核外电子排布规律可知,第1层有2个电子,第2层有8个电子,第3层有1个电子。钠元素的原子结构示意图为 ,不符合题意。
,不符合题意。
故选A。

 暑假作业暑假快乐练西安出版社系列答案
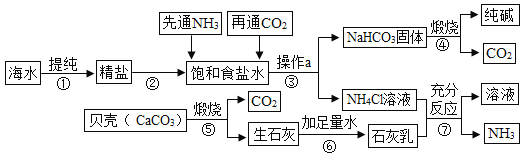
暑假作业暑假快乐练西安出版社系列答案【题目】我国化学家侯德榜创立的侯氏制碱法为纯碱工业技术发展做出杰出贡献。在制备纯碱过程中涉及Na2CO3、NaCl、NH4Cl、NaHCO3等物质。请结合下表数据回答:
温度/°C | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | Na2CO3 | 7 | 12.2 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | |
(1)在50°C时,向100g水中加入48gNa2CO3充分搅拌所得溶液质量为____,保持烧杯中各物质质量不变,降温至40°C时,所得溶液溶质的质量分数会____(填“变小”、“不变”或“变大”)。
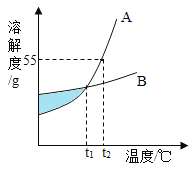
(2)请根据表格中数据在如图中绘制Na2CO3溶解度曲线____。
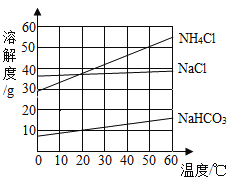
(3)根据图中四种物质的溶解度曲线,回答下列问题:
①60°C时,分别向等质量的四种固体物质中加水配成饱和溶液,所得溶液质量最大的是_____。
②侯氏制碱法的原理是:NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3,在生成物碳酸氢钠和氯化铵中,先析出的是____,理由是____。
【题目】如表是甲、乙两种固体(不含结晶水)在不同温度下的溶解度(单位:g/100g水)
温度(°C) | 0 | 20 | 40 | 60 | 80 | 90 | 100 |
甲 | 13.3 | 32 | 64 | 110 | 169 | 202 | 246 |
乙 | 35.7 | 36 | 36.6 | 37.3 | 38.4 | 39 | 39.8 |
(1)60°C时甲的溶解度为______,将60g甲放入50g水中充分溶解得到溶液________g。
(2)从乙的溶液中提取乙的方法是_______(选填“降温结晶”或“蒸发结晶”)。
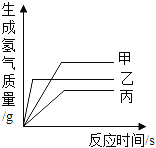
(3)分别将100g甲、乙的饱和溶液从60°C降温至20°C,对所得溶液的叙述正确的是______
A.甲、乙均为饱和溶液
B.溶液质量:甲>乙
C.所含溶剂质量:甲<乙
D.溶质质量分数:甲>乙