题目内容
【题目】向100g溶质质量分数为14.6%的稀盐酸溶液,加入一定质量的Na2CO3溶液,充分反应后 得到仍含HCl质量分数3.65%的混合溶液200g。
(1)参加反应的HCl质量为_____g;
(2)所加入Na2CO3溶液的溶质质量分数为__________________?(写出计算过程,结果保留0.1%)
(3)若要使反应后的混合溶液中HCl质量分数恢复到14.6%,需要向混合溶液中通入并溶解HCl气体___________g(结果保留0.1g)。
【答案】7.3 10.2% 21.9
【解析】
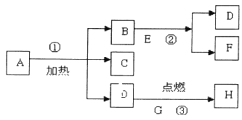
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断。
解:(1)参加反应的HCl质量为:100g×14.6%-200g×3.65%=7.3g;
(2)设反应的碳酸钠质量为x,生成二氧化碳质量为y,
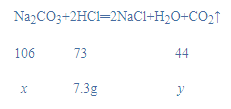
![]() x=10.6g,
x=10.6g,
![]() y=4.4g,
y=4.4g,
碳酸钠溶液质量为:200g-100g+4.4g=104.4g,所加入Na2CO3溶液的溶质质量分数为:![]() ×100%=10.2%,
×100%=10.2%,
(3)若要使反应后的混合溶液中HCl质量分数恢复到14.6%,需要向混合溶液中通入并溶解HCl气体质量为:200g×14.6%-7.3g=21.9g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
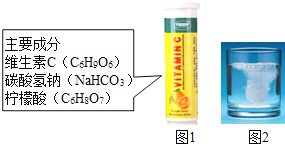
小学生10分钟应用题系列答案【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO_____________________________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有_________,写出该反应的化学方程式________________。
(2)由实验②____________(填“能”或“不能”)确定该气体中不含氧气,理由是______________________。
探究二:维C泡腾片溶液的酸碱性。
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显_________性。