题目内容
【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
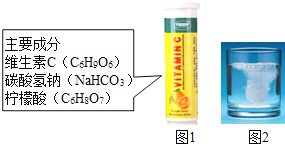
探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO_____________________________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有_________,写出该反应的化学方程式________________。
(2)由实验②____________(填“能”或“不能”)确定该气体中不含氧气,理由是______________________。
探究二:维C泡腾片溶液的酸碱性。
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显_________性。
【答案】根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含氮元素。有毒。
(1)二氧化碳;Ca(OH)2+CO2=CaCO3↓+H2O。
(2)不能;若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃。酸。
【解析】【猜想与假设】根据图示维C泡腾片的成分可知,其中含有C、H、O、Na等元素,不含N元素。结合在化学反应前后元素种类不变。可进行解答。
一氧化碳进入人体之后会和血液中的血红蛋白结合,进而使血红蛋白不能与氧气结合,从而引起机体组织出现缺氧,导致人体窒息死亡。因此一氧化碳具有毒性。
【得出结论】(1)根据题中“将气体通入澄清的石灰水中”出现的现象“澄清石灰水变浑浊”,可知该气体为二氧化碳。澄清石灰水的主要成分为氢氧化钙,所以反应为:Ca(OH)2+CO2=CaCO3↓+H2O
(2)当氧气的浓度达到一定程度(50%)后,才能使木条复燃。当氧气含量过少时,带火星的木条不能复燃。所以本题中木条未复燃,不能说明是否含有氧气。
探究二:石蕊遇酸变红(PH<5.0),遇碱变蓝。根据题中描述,可判断溶液显酸性

 教材全解字词句篇系列答案
教材全解字词句篇系列答案