题目内容
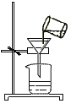
【题目】下图是实验室制取二氧化碳气体的装置图。请你运用所学化学知识回答下列问题:
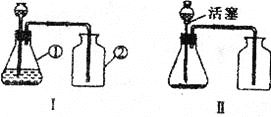
(1)图中仪器①的名称是__________;仪器②的名称是__________。
(2)制取二氧化碳气体前,首先要检查装置的__________。
(3)在实验室里,制取二氧化碳不用Na2CO3代替大理石做反应原料的原因是__________。
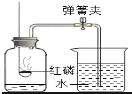
(4)小红根据实验室制取二氧化碳气体的反应原理,设计了如图装置Ⅱ,装置Ⅱ与装置I相比较,你认为装置__________(填“Ⅰ”或“Ⅱ”)更好一些,理由是____________________。
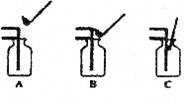
(5)在实验室里,常用__________法收集二氧化碳气体,检验的方法是__________。小红又设计了如图三种装置,用三种不同方法验证二氧化碳气体是否收集满。你认为,选__________装置更为合理。
【答案】锥形瓶 集气瓶 气密性 碳酸钠与盐酸反应速率太快(或不易控制反应的进行或不便于实验操作) Ⅱ 能随时控制滴加液体的量(或速度) 向上排空气 用燃着的木条放在集气瓶口,看木条是否熄灭 B
【解析】
(1)据图可知仪器①是长颈漏斗,②是集气瓶;
(2)制取二氧化碳气体前,首先要检查装置的气密性;
(3)实验室常用稀盐酸和大理石反应制取二氧化碳气体,不用碳酸钠代替大理石作反应原料的原因:反应速率太快,不利气体收集;
(4)根据实验室制取二氧化碳气体的原理,装置Ⅱ与装置Ⅰ比较,Ⅱ更好一些,理由是:可控制酸液的滴加量及滴加速度;
(5)因为二氧化碳的密度比空气大,可以用向上排空气法收集;二氧化碳的密度比空气大,不能燃烧,不支持燃烧,检验是否收集满时应该把燃烧的木条放在集气瓶口,B装置更为合理。

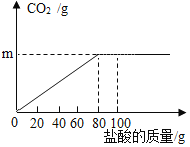
【题目】钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂主要成分为碳酸钙,现将100g盐酸分成5等份,逐次加到用40g该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图像。请根据有关信息回答问题
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入盐酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
剩余固体的质量(g) | 35 | 30 | 25 | 20 | a |
(1)求碳酸钙中各元素的质量比Ca:C:O=___________。(化成最简整数比)
(2)a的数值为_______,该品牌补钙药剂中CaCO3的质量分数是_______
(3)求该盐酸中溶质的质量分数_______(写出计算过程,计算结果保留一位小数)。