题目内容
2C2H5OH的总相对分子质量为 .等质量的SO2和SO3中氧元素的质量比为 ;要使SO2和SO3的含氧量相等,则SO2和SO3的质量比是 .
分析:根据相对分子质量为构成分子的各原子的相对原子质量之和,化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:2C2H5OH的总相对分子质量为(12×2+1×5+16×5)×2=92.
设相同质量的SO2和SO3的质量为m,则所含氧元素的质量比为(m×
×100%):(m×
×100%)=5:6.
要使SO2和SO3含有相同质量的氧元素,则氧原子的个数应相等,3SO2和2SO3中氧原子个数相等,则SO2和SO3的质量比(3×64):(2×80)=6:5.
故答案为:92;5:6;6:5.
设相同质量的SO2和SO3的质量为m,则所含氧元素的质量比为(m×
| 16×2 |
| 32+16×2 |
| 16×3 |
| 32+16×3 |
要使SO2和SO3含有相同质量的氧元素,则氧原子的个数应相等,3SO2和2SO3中氧原子个数相等,则SO2和SO3的质量比(3×64):(2×80)=6:5.
故答案为:92;5:6;6:5.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
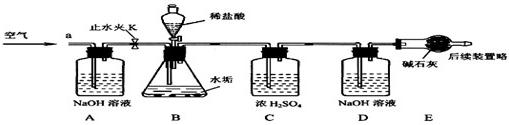
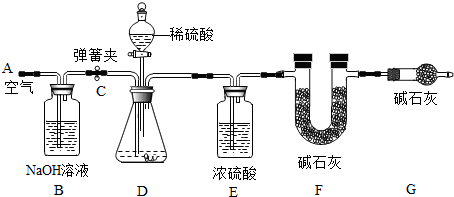
 中国石油天然气集团公司近日宣布,在渤海湾滩海地区发现储量规模达十亿吨的大油田--冀东南堡油田.这对增强我国能源安全供应的保障能力具有重要意义.石油中主要含有碳和氢两种元素,利用石油中各成分的沸点不同,将它们分离(称为分馏),可得到不同的产品,使石油得到综合利用(如图).
中国石油天然气集团公司近日宣布,在渤海湾滩海地区发现储量规模达十亿吨的大油田--冀东南堡油田.这对增强我国能源安全供应的保障能力具有重要意义.石油中主要含有碳和氢两种元素,利用石油中各成分的沸点不同,将它们分离(称为分馏),可得到不同的产品,使石油得到综合利用(如图).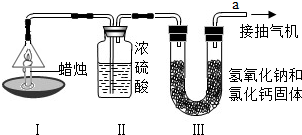
 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.