题目内容
用锌片与稀硫酸反应制H2,每次实验结果记录如下:|
次数 |
加入锌片的质量 |
稀硫酸 |
产生H2质量 |
|
1 |
6.5 g |
100 g |
0.2 g |
|
2 |
13 g |
100 g |
|
|
3 |
19.5 g |
100 g |
0.6 g |
|
4 |
26 g |
100 g |
0.8 g |
|
5 |
32.5 g |
100 g |
|
|
6 |
39 g |
100 g |
0.8 g |
(1)第二、五次产生的氢气质量是多少?
(2)35 g锌片与100 g这种稀硫酸充分反应后,所得溶液的溶质质量分数为多少?
(3)稀硫酸的溶质质量分数为多少?
答案:
解析:
解析:
| 答案:(1)0.4 g 0.8 g
根据表分析,26 g锌片时产生的氢气就已达到最大值,此时锌片就已过量或刚好,所以35 g锌片肯定过量,硫酸完全反应,这时产生的H2的质量为0.8 g. 解:设反应的锌的质量为x,硫酸的质量为y. Zn+H2SO4===ZnSO4+H2↑ 65 98 2 x y |



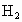 ,完全反应后,所需时间与当地金属价格见表.你认为实验室一般不选用铁屑、镁片与酸反应制氢气的主要原因是什么?
,完全反应后,所需时间与当地金属价格见表.你认为实验室一般不选用铁屑、镁片与酸反应制氢气的主要原因是什么?

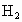 ,完全反应后,所需时间与当地金属价格见表.你认为实验室一般不选用铁屑、镁片与酸反应制氢气的主要原因是什么?
,完全反应后,所需时间与当地金属价格见表.你认为实验室一般不选用铁屑、镁片与酸反应制氢气的主要原因是什么?
