题目内容
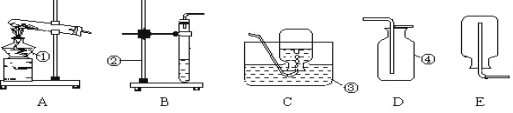
【题目】下图是实验室制取二氧化碳并试验其性质的装置和操作示意图。
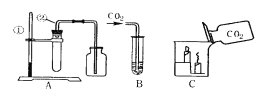
试回答下列有关问题:
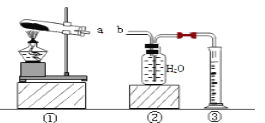
(1)写出仪器①和②的名称:①是________,②是________。
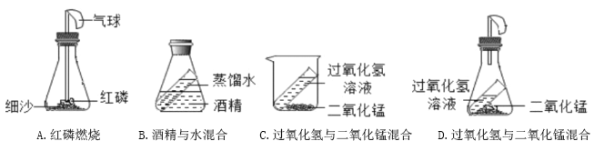
(2)A中制取二氧化碳的化学方程式是______。
(3)为了检验A装置的集气瓶里是否充满二氧化碳,可用燃着的火柴放在__________进行实验,如果火焰熄灭,证明已经充满。
(4)若B的试管里盛的是紫色石蕊试液,观察到的现象是________;发生反应的化学方程式是_____。
(5)C所示的实验说明了二氧化碳具有哪些性质?____________。
【答案】铁架台 导管 CaCO3+2HCl==CaCl2+H2O+CO2↑ 瓶口 变红 CO2 + H2O =H2CO3 密度比空气大,不能燃烧,也不能支持燃烧
【解析】
(1) 仪器①名称是铁架台,故填铁架台;仪器②的名称是导管,故填导管。
(2)制取二氧化碳的药品是石灰石和稀盐酸,反应是碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,故化学方程式写为:CaCO3+2HCl==CaCl2+H2O+CO2↑。
(3)验满二氧化碳的方法是将燃着的火柴放在瓶口处,如果火焰熄灭,证明已经充满,故填瓶口。
(4)二氧化碳与水反应生成碳酸,碳酸溶液显酸性,能使紫色石蕊试液变成红色,故填液体变红;反应是水与二氧化碳反应生成碳酸,故化学方程式写为:CO2 + H2O =H2CO3。
(5)C处的现象是下层蜡烛先熄灭,上层蜡烛后熄灭,蜡烛熄灭说明二氧化碳不能燃烧,也不能支持燃烧;下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳的密度大于空气的密度,故填密度比空气大,不能燃烧,也不能支持燃烧。

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案
相关题目