题目内容
【题目】硫酸是化学实验室里的常见试剂.现利用质量分数为98%、密度为1.84g/cm3的浓硫酸配制100mL质量分数为10%、密度为1.07g/cm3的稀硫酸.(已知:水的密度近似为1g/cm3,不同质量分数的溶液混合后总体积不是两种溶液体积之和)
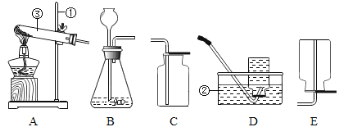
(1)量取浓硫酸时需要的仪器是_______.

(2)配制该稀硫酸溶液时,下列方法最合理的是_______(假设需要浓硫酸的体积是V mL).
a分别用量筒量取V mL浓硫酸和(100﹣V)mL水,在烧杯中混合均匀
b先量取V mL浓硫酸倒入烧杯中,再称量(107﹣1.84V)g水,慢慢倒入盛有浓硫酸的烧杯中混合均匀
c先量取(107﹣1.84V)mL水倒入烧杯中,再将量取的V mL浓硫酸慢慢倒入盛水的烧杯中混合均匀
d先在100mL量筒中加入V mL浓硫酸,然后向其中加水恰好至100mL刻度处混合均匀
(3)在量取浓硫酸时若俯视量筒的刻度线,则所配制的硫酸溶液的质量分数_______10%(填“大于”、“等于”或“小于”).
(4)用pH试纸测定所配制的硫酸溶液的pH,正确的操作是_______.
【答案】D c 小于 撕一小段pH试纸置于表面皿中,用玻璃棒蘸取试液滴在pH试纸上,再与标准比色卡对照读出pH值
【解析】
(1)由m=ρV和溶液在配制前后溶质的质量不变,
设需要浓硫酸的体积为V,则
![]()
解得V=6.6mL;
根据量程相近的原则,量取浓硫酸时需要的仪器是10mL量筒,D选项正确,符合题意;
(2)稀释浓硫酸为防止产生的热量造成液体迸溅,要及时散热,则将密度大的液体加到密度小的液体中并用玻璃棒搅拌来散热,配制该稀硫酸溶液时,加水的质量为![]() ,
,
最合理的方法是:先量取![]() mL水倒入烧杯中,再将量取的V mL浓硫酸慢慢倒入盛水的烧杯中混合均匀;
mL水倒入烧杯中,再将量取的V mL浓硫酸慢慢倒入盛水的烧杯中混合均匀;
(3)用量筒量取浓硫酸时俯视刻度,看到的读数偏大,但量取的实际体积偏小,也就是说溶质少了,而量取水时却仰视体积读数,看到的读数偏小,但量取的实际体积偏大,也就是说溶剂多了;所以所配溶液的溶质质量分数比实际偏小;
(4)测定溶液pH的具体操作方法为:撕一小段pH试纸置于表面皿中,用干净的玻璃棒蘸取待测溶液并滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出相同颜色的pH值。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案