题目内容
取一定质量的CO和CO2的混合气体,通入足量Ba(OH)2溶液中,充分反应后过滤,发现生成的沉淀和所取的混合气体质量相等,则混合气体中,碳原子与氧原子的物质的量之比为( )A.181:209
B.28:44
C.1:2
D.1:1
【答案】分析:CO和CO2的混合气体,通入足量的Ba(OH)2溶液中,充分反应后过滤,所得沉淀为二氧化碳与氢氧化钡反应生成碳酸钡;生成的沉淀和所取的混合气体质量相等,即生成碳酸钡的质量与混合气体的质量相等.通过假设碳酸钡的质量,根据反应化学方程式,求得混合气体中所取CO和CO2的混合气体中质量关系,从而利用两气体中C、O元素质量比得出混合气体中C、O元素质量关系,最后利用C、O元素的相对原子质量求出混合气体中碳原子与氧原子的物质的量之比.
解答:解:假设充分反应后生成碳酸钡的质量为197g,
设混合气体中二氧化碳质量为x
CO2+Ba(OH)2═BaCO3↓+H2O
44 197
x 197g

x=44g
则混合气体中CO的质量=197g-44g=153g
则混合气体中C、O元素质量比=(44g× +153g×
+153g× ):(44g×
):(44g× +153g×
+153g× )=543:836
)=543:836
混合气体中碳原子与氧原子的物质的量之比= :
: =181:209
=181:209
故选A
点评:由于题中生成的沉淀和所取的混合气体质量相等,该问题的焦点集中到混合气体的质量与反应生成的碳酸钡的质量上,如果有了碳酸钡的质量,一切问题都会迎刃而解.
解答:解:假设充分反应后生成碳酸钡的质量为197g,
设混合气体中二氧化碳质量为x
CO2+Ba(OH)2═BaCO3↓+H2O
44 197
x 197g

x=44g
则混合气体中CO的质量=197g-44g=153g
则混合气体中C、O元素质量比=(44g×
 +153g×
+153g× ):(44g×
):(44g× +153g×
+153g× )=543:836
)=543:836混合气体中碳原子与氧原子的物质的量之比=
 :
: =181:209
=181:209故选A
点评:由于题中生成的沉淀和所取的混合气体质量相等,该问题的焦点集中到混合气体的质量与反应生成的碳酸钡的质量上,如果有了碳酸钡的质量,一切问题都会迎刃而解.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
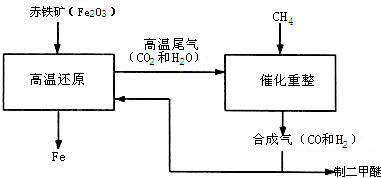
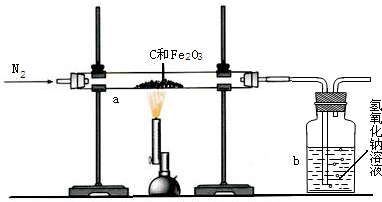
 某研究性学习小组设计并进行了如下实验.
某研究性学习小组设计并进行了如下实验.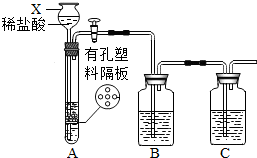 某研究性学习小组设计并进行了如下实验.
某研究性学习小组设计并进行了如下实验.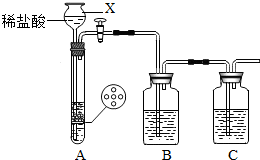 (2012?崇川区一模)某研究性学习小组设计并进行了如下实验.
(2012?崇川区一模)某研究性学习小组设计并进行了如下实验. 某研究性学习小组设计并进行了如下实验.
某研究性学习小组设计并进行了如下实验.