��Ŀ����
 ij�о���ѧϰС����Ʋ�����������ʵ�飮
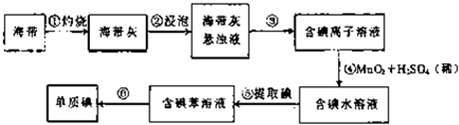
ij�о���ѧϰС����Ʋ�����������ʵ�飮��1������ͬѧ����ͼװ����ȡ���﴿���Ķ�����̼���壮��ش��������⣺
������X��������
����©��
����©��
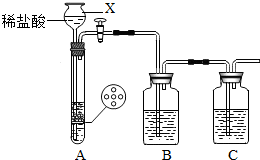
��ʵ��ǰ���رջ�������X�м���ˮʹX��Һ������Թ��е�Һ�棬һ��ʱ���Һ�汣�ֲ���˵��Aװ�õ�����������
Aװ�õ�����������
����Ϊ��ȥCO2�л��е�HCl���壬Bװ����ʢ�ű���NaHCO3��Һ��д���÷�Ӧ�Ļ�ѧ����ʽ
NaHCO3+HCl=NaCl+CO2��+H2O
NaHCO3+HCl=NaCl+CO2��+H2O
����Ҫ�õ������CO2��Cװ��Ӧʢ��
Ũ����
Ũ����
�����Լ����ƣ�������˵��װ��B��C���Լ����ܽ�����ԭ��
��������������ͨ������NaHCO3��Һ��������ˮ��������
��������������ͨ������NaHCO3��Һ��������ˮ��������
����2������ͬѧΧ��CO��ԭCuO�����ĺ�ɫ�����Ƿ�һ����Cu����̽����
���������ϡ�
��Cu2O��ĩ�ʺ�ɫ����������Һ�У�Cu2O+H2SO4=Cu+CuSO4+H2O
���ڿ����и�������ʱ��Cu2O�ȶ�����CuO���ֽ�����Cu2O��O2
��������롿
�����ɫ������Cu�� �����ɫ������Cu2O�� �����ɫ������
Cu2O��Cu�Ļ����
Cu2O��Cu�Ļ����
����ʵ��̽����
�����д����Cu����Cu2O�Ļ�ѧ����ʽ��
4Cu+O2
2Cu2O
| ||
4Cu+O2
2Cu2O
��
| ||
��������ݷ���
��1��ȡһ�������ĺ�ɫ����a g���ڿ����и������գ�ֱ���������ٷ����ı䣬�������ù�������Ϊb g��
����a=b�������
II
II
����������b��a����˵����ɫ������һ������
Cu
Cu
���ʣ���2����ȡ������ɫ����Ͷ��ϡ�����У���ַ�Ӧ����Һ����ɫ�����ݴ�����˵���˺�ɫ�����к���
Cu2O
Cu2O
������������1.6g��ԭ���������ϡ���ᷢ����Ӧ��������2.88
2.88
g����������1���ٸ������������ƺ������Լ�鷽�����ǣ��ڸ��ݷ���ʽ��д�����ǣ��۸���Ũ�������ˮ�Կ��ǣ��ܸ��ݵ���������ĺ�����ǣ���2����������������ʶ��п��ǣ���ʵ��̽����������ݷ���ʽ��д�����ǣ���1������ͭ��������ͭ�������պ������ĸñ������ǣ���2������������ͭ�����ᷴӦ����ͭ�����������ļ��������м��㣮
����⣺��1���پ��Ƚϳ��������dz���©�����رջ�������X�м���ˮʹX��Һ������Թ��е�Һ�棬һ��ʱ���Һ�汣�ֲ���˵��Aװ�ò�©��������ȡ����ǰ�����ȼ��װ�õ������ԣ���������©���ռ��������壻
������ͨ��Bװ��ʱ������Ӧ�ķ�Ӧ����̼�����ƺ����ᣬ���������Ȼ��ơ�ˮ�Ͷ�����̼��������̼��������������ţ�
������Ũ���������ˮ�ԣ�����Ҫ�õ������CO2��ͨ��Ũ���ἴ�ɣ�
����������������ͨ������NaHCO3��Һ������̼��������Һ�к���ˮ����������ˮ���������ˣ�
��2�������ɫ���������Cu��������Cu2O������һ�ֿ��ܾ��Ƕ��߶��У�
��ʵ��̽���������Ӧ����ͭ����������������������ͭ���ù۲취��ƽ����Ӧ�����Ǽ���д�ڵȺŵ��ϱߣ�
��1��������Cu2O�����ȶ������������䣬ͭ���Ⱥ��Ϊ������ͭ�����������˱仯��������a=b˵�������������䣬������������ͭ��
����b��a˵���������������ˣ�һ������ͭ����Ϊͭ��������Ӧ����������ͭ�������������
��2��ȡ������ɫ����Ͷ��ϡ�����У���ַ�Ӧ����Һ����ɫ��˵����ɫ�����������ᷴӦ��ͭ�������Ӧ������˵���˺�ɫ�����к���������ͭ��
��������ͭ����ΪX��
Cu2O+H2SO4=Cu+CuSO4+H2O
144 64 ������������80
X ��������1.6g
���ݣ�
=
���X=2.88g��
�ʴ�Ϊ����1���ٳ���©����Aװ�õ����������ã���NaHCO3+HCl=NaCl+CO2��+H2O����Ũ��� ����������������ͨ������NaHCO3��Һ��������ˮ������������2����������롿Cu2O��Cu�Ļ�����ʵ��̽����4Cu+O2
2Cu2O��II��Cu��Cu2O��2.88��
������ͨ��Bװ��ʱ������Ӧ�ķ�Ӧ����̼�����ƺ����ᣬ���������Ȼ��ơ�ˮ�Ͷ�����̼��������̼��������������ţ�
������Ũ���������ˮ�ԣ�����Ҫ�õ������CO2��ͨ��Ũ���ἴ�ɣ�
����������������ͨ������NaHCO3��Һ������̼��������Һ�к���ˮ����������ˮ���������ˣ�
��2�������ɫ���������Cu��������Cu2O������һ�ֿ��ܾ��Ƕ��߶��У�
��ʵ��̽���������Ӧ����ͭ����������������������ͭ���ù۲취��ƽ����Ӧ�����Ǽ���д�ڵȺŵ��ϱߣ�
��1��������Cu2O�����ȶ������������䣬ͭ���Ⱥ��Ϊ������ͭ�����������˱仯��������a=b˵�������������䣬������������ͭ��
����b��a˵���������������ˣ�һ������ͭ����Ϊͭ��������Ӧ����������ͭ�������������
��2��ȡ������ɫ����Ͷ��ϡ�����У���ַ�Ӧ����Һ����ɫ��˵����ɫ�����������ᷴӦ��ͭ�������Ӧ������˵���˺�ɫ�����к���������ͭ��
��������ͭ����ΪX��
Cu2O+H2SO4=Cu+CuSO4+H2O
144 64 ������������80
X ��������1.6g
���ݣ�
| 144 |
| 80 |
| X |
| 1.6g |
�ʴ�Ϊ����1���ٳ���©����Aװ�õ����������ã���NaHCO3+HCl=NaCl+CO2��+H2O����Ũ��� ����������������ͨ������NaHCO3��Һ��������ˮ������������2����������롿Cu2O��Cu�Ļ�����ʵ��̽����4Cu+O2
| ||
�������������׳����ĵط���������ͭ������������ͭ�������Ӧ��������ͭ�����ᷴӦ������ͭ������ͭ��ˮ������������ͭͨ����Ӧ����ͭ�����Թ����������٣����ݲ�ֵ�����м��㼴�ɣ�

��ϰ��ϵ�д�
�����Ŀ
 ��2012?�紨��һģ��ij�о���ѧϰС����Ʋ�����������ʵ�飮
��2012?�紨��һģ��ij�о���ѧϰС����Ʋ�����������ʵ�飮
 ij�о���ѧϰС����Ƶ�ʵ��װ�ã���ͼ�����ȿ���ȡ���壬�ֿ�������֤�������ʣ�
ij�о���ѧϰС����Ƶ�ʵ��װ�ã���ͼ�����ȿ���ȡ���壬�ֿ�������֤�������ʣ�